Закись - азот
Cтраница 1
 |
Растворимость ( объем газа / объем H2SO закиси азота NSO в растворах серной кислоты. [1] |
Закись азота - соединение непрочное, легко разлагающееся при 170 С ( 443 К) на элементарные азот и кислород. [2]
Закись азота и сероокись углерода встречаются в природных газах лишь в малых концентрациях. [3]
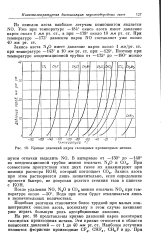 |
Кривые давлений паров галоидных производных метана. [4] |
Закись азота при этом растворяется лишь незначительно, если определение провести быстро, не допуская долгого стояния газа в пипетке с КОН. [5]
Закись азота открыта Пристлеем в 1772 г. Вдыхание веселящего газа сделалось одно время чрезвычайно модным среди публики, специально приезжавшей к Дэви подышать удивительным газом. [6]
Закись азота - бесцветный газ, имеет сладковатый вкус и слабый, приятный запах. Интересуясь действием различных газов на организм человека, Дэви обычно испытывал их на себе. [7]
Закись азота N2O действует практически как индифферентный газ, а в очень больших концентрациях в смеси с кислородом - как наркотик. Окись азота NO вызывает быстрое превращение гемоглобина крови в метгемоглобин и действует на центральную нервную систему. Нитриты, а также эфиры азотистой кислоты сильно расширяют сосуды и снижают кровяное давление и переводят гемоглобин крови в метгемоглобин. Эфиры азотной кислоты действуют наркотически, поражают сердечно-сосудистую систему, а также образуют метгемоглобин. [8]
Закись азота сравнительно нереакционноспособна, причем при комнатной температуре она инертна по отношению к галогенам, щелочным металлам и озону. При более высоких температурах разлагается на азот и кислород, реагирует со щелочными металлами и многими органическими соединениями и поддерживает горение. Умеренно растворима в кремах и, если не учитывать важности в качестве анестезирующего вещества, находит промышленное применение в качестве пропеллента в кремовых бомбах. [9]
Закись азота имеет много областей поглощения, простирающихся до длин волн, больших 2100 А. Химические продукты, несомненно, - одни и те же независимо от использованной спектральной области поглощения, но электронные состояния основных образующихся частиц изменяются при переходе от области к области. [10]
Закись азота и двуокись углерода имеют одинаковое число электронов, и можно было бы надеяться, что их линейность поможет разрешить спектр и дать его надежную интерпретацию. И несмотря на достигнутые в этом направлении значительные успехи, все же кое-что еще не ясно. Поскольку в линейной молекуле один тип колебаний дважды вырожден, эффективное число колебательных степеней свободы линейной молекулы равно ( Зп - 5), где п - количество атомов в молекуле. [11]
Закись азота представляет собою бесцветный газ со слабым запахом и сладковатым вкусом. [12]
Закись азота - термодинамически неустойчивое соединение. [13]
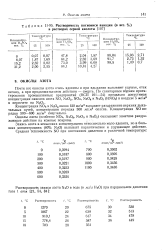 |
Растворимость пятиокиси ванадия ( в вес. % в растворах серной кислоты. [14] |
Закись азота в невысоких концентрациях относительно мало ядовита, но в больших концентрациях ( 80 % N2O) вызывает наркотическое и удушающее действие. [15]
Страницы: 1 2 3 4