Кинетика - поликонденсация
Cтраница 1
Кинетика поликонденсации аналогична кинетике конденсации соответствующих ( или близких по строению) простых молекул. [1]
Кинетика поликонденсации в расплаве в присутствии катализатора становится более сложной, чем в его отсутствие: в ряде случаев реакция начинает описываться уравнением не второго порядка. Изменение порядка реакции происходит в том случае, если каталитическими свойствами обладает один из реагентов. Так, поликонденсация карбоновых кислот с диолами катализируется анионами. [3]
Кинетика поликонденсации ( ди 3-оксиэтил) - себацината. [4]
Кинетика поликонденсации этих исходных веществ была изучена в среде динила в интервале 110 - 150 С при эквимолекулярном соотношении исходных веществ. [5]
Кинетика поликонденсации в каждой из фаз зависит от концентрации и химической природы обоих исходных веществ. Концентрация же исходных веществ в фазе определяется их общей концентрацией, коэффициентом распределения, скоростью диффузии мономеров. Таким образом, изучение кинетики межфазной поликонденсации весьма трудно с экспериментальной точки зрения. Именно этим и объясняются немногочисленные данные в этой области. [6]
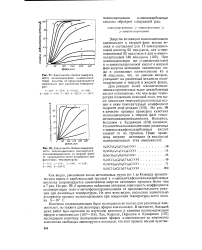 |
Зависимость степени завершенности поликонденсации ю-аминоэнан-товой кислоты от продолжительности нагревания при различных температурах. [7] |
Кинетика поликонденсации была исследована не только для различных аминокислот, но также и для некоторых эфиров аминокислот. [8]
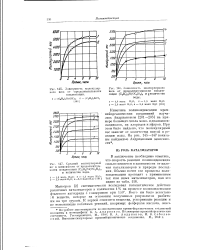 |
Зависимость молекулярного веса от продолжительности конденсации.| Средний молекулярный вес в зависимости от продолжительности конденсации ( С2Н5 В1 ( ОС2Н5 з и количества води. [9] |
Кинетика поликонденсации крем-нийорганических соединений изучалась Андриановым [201-203] на примере большего числа моно - и диалкилси-ландиолов, их хлоридов и эфиров. [10]
Кинетика поликонденсации этилового эфира глицина была исследована Хургиным, Порошиным и Козаренко [21], которые установили, что промежуточными продуктами реакции являются эфиры N-карбокси-сс - аминокислот, представляющие истинные мономеры реакции. [11]
Изучение кинетики поликонденсации важно с двух точек зрения. Для практического синтеза высокомолекулярных полимеров нужно знать кинетику процесса его образования. С теоретических позиций граница между полимеризацией и полпкон-денсацией во многом определяется особенностями их кинетики. [12]
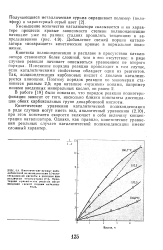
Изучение кинетики поликонденсации ы-аминокислот в твердой фазе показало, что реакция имеет автокаталитический характер, т.е. ускоряется по мере прохождения реакции. Это объясняется, по-видимому, тем, что при протекании поликонденсации увеличивается поверхность раздела мономер - полимер, на которой молекулы мономера имеют подвижность, необходимую для протекания поликонденсации. Экспериментально установлена зависимость скорости поликонденсации от величины кристаллов мономеров: с увеличением размера кристаллов возрастает как средняя, так и максимальная скорость поликонденсации. [13]
Изучение кинетики поликонденсации хлорангидрида терефталевой кислоты с перечисленными полимерными блочными компонентами показало, что все они обладают достаточной реакционной способностью, чтобы быть использованными для синтеза смешанных блок-полиарилатов, однако, как это было уже показано на стр. [14]
Рассмотрим кинетику поликонденсации на примере образования полиэфира из гликоля и двухосновной кислоты. Обычно в этой реакции катализатором служит сильная кислота. Однако если ее не добавляют, то исходная двухосновная кислота сама оказывает каталитическое действие. [15]
Страницы: 1 2 3 4 5