Активная концентрация - ион - водород
Cтраница 1
Активная концентрация ионов водорода в воде зависит от химического состава и концентрации веществ, содержащихся в этой воде. При этом рН природной воды в подавляющем большинстве случаев зависит главным образом от соотношения различных форм углекислоты, содержащейся в воде. По величине рН, как показано в § 40, можно вычислить соотношение между различными формами углекислоты, если известно общее содержание углекислоты в данной воде. [1]
Активная концентрация ионов водорода ( рН) в пароводяном цикле ТЭС оценивается потенциомстрическим методом. [2]
Находим активную концентрацию ионов водорода в данном растворе. [3]
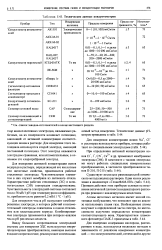 |
Технические данные кондуктометров. [4] |
Для измерения активной концентрации ионов водорода в растворе, определяющей его кислотные или щелочные свойства, применяются рабочие стеклянные электроды. Чувствительным элементом в них служит мембрана из литиевого стекла. Характеристики рабочих стеклянных ( ЭС) и вспомогательных ( ЭВ) электродов стандартизованы. [5]
Для определения активной концентрации ионов водорода ( или рН) составляем цепь из стандартного водородного электрода ( см. рис. 122) и неизвестного водородного электрода, электролитом в котором служит исследуемая жидкость. [6]
Таким образом, активная концентрация ионов водорода может обобщенно характеризовать кислотные или щелочные свойства растворов. Вместо того чтобы характеризовать кислотность или щелочность раствора водородным числом, пользуются логарифмом этого числа с отрицательным знаком. [7]
Колориметрический метод определения активной концентрации ионов водорода основан на применении веществ, называемых индикаторами, окраска которых зависит от рН раствора. [8]
Предназначен для определения активной концентрации ионов водорода в водных растворах. Применяется в заводских лабораториях и научно-исследовательских институтах. Работает со вторичными приборами ЭПП-09 или ЭПД. [9]
 |
Сурьмяный электрод. [10] |
Потенциал электрода определяется активной концентрацией ионов водорода в соприкасающейся с ним среде. [11]
Состояние этих равновесий, очевидно, определяется активной концентрацией ионов водорода в данной воде. В общем здесь наблюдается полная аналогия с рассмотренными выше ( § 39 и 40) равновесиями между различными формами углекислоты и разница будет только в величинах констант диссоциации. [12]
 |
Зависимость ЭДС от рН. [13] |
ЭДС цепи в целом изменяются пропорционально отрицательному логарифму активной концентрации ионов водорода в растворе. Прямолинейность функции Е от lg n является характерной особенностью концентрационных цепей и отдельных электродов. [14]
Очень широко применяются цепи с водородным электродом для определения активной концентрации ионов водорода в различных растворах и средах ( стр. [15]
Страницы: 1 2 3