Парциальный молярный объем
Cтраница 1
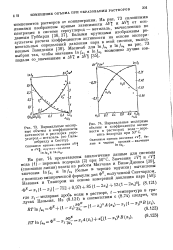 |
Парциальные молярные объемы и коэффициенты активности в растворах сероуглерод - метилаль ( но Гиль. [1] |
Парциальные молярные объемы и коэффициенты активности в растворах вода - перекись водорода при 50 С. [2]
 |
Зависимость интегральной теплоты растворения H. jSO4 в воде от соотношения молей воды в кислоты. [3] |
Парциальные молярные объемы тем больше отличаются от объемов компонентов в чистом состоянии, чем более разбавлен раствор. Кажущиеся объемы тем меньше отличаются от парциальных молярных, чем более разбавлен раствор. [4]
Парциальные молярные объемы и в жидкой и в паровой фазах зависят от состава реального раствора, поэтому константы фазового равновесия АН являются функциями не только р и Т, по и концентрации г-го компонента. [5]
Парциальные молярные объемы можно определить обычными экспериментальными методами; если это необходимо и удобно, данные о парциальных объемах интересующих компонентов можно рассчитать, используя результаты определения парциальных объемов только одного компонента, например, растворителя, во всей области составов. Что касается производных, то для их расчетов необходимо располагать данными о зависимости величин Р от состава ионита в изотермо-изобарических условиях. [6]
Парциальные молярные объемы при температурах выше 25 С были определены только для диоксида углерода и метана. [7]
Парциальные молярные объемы и в жидкой и в паровой фазах зависят от состава реального раствора, поэтому константы фазового равновесия АН являются функциями не только р и 7 но и концентрации г-го компонента. [8]
Парциальные молярные объемы и кажущиеся молярные объемы определяются нз значений плотностей растворов. [9]
Парциальные молярные объемы и кажущиеся молярные объемы определяются из значений плотностей растворов. [10]
Парциальные молярные объемы можно найти, если молярный объем раствора известен как функция состава раствора при постоянных давлении и температуре. [11]
Парциальный молярный объем сорбата в растворе. [12]
Парциальный молярный объем при бесконечном разбавлении относится к кажущемуся молярному объему так же как производная ( отношение двух бесконечно малых величин) к отношению конечных приращений. Кажущийся молярный объем представляет собой средний парциальный молярный объем между его значениями при бесконечном разведении и при концентрации раствора, образующегося в процессе прибавления конечного числа молей п2 к растворителю. [13]
Обычно парциальные молярные объемы в многокомпонентных системах неизвестны. Поэтому вводится понятие идеального раствора ( см. раздел 6) и тогда принимают, что парциальные молярные объемы веществ в системе равны молярным объемам чистых веществ. [14]
Парциальный молярный объем растворителя находим следующим образом. [15]
Страницы: 1 2 3 4