Потенциометрическое определение
Cтраница 1
Потенциометрические определения не ограничены только этими двумя катионами. [1]
Потенциометрические определения рН получили широкое распространение благодаря высокой точности и возможности применять их к сложным системам, для которых колориметрические и другие методы не могут дать удовлетворительных результатов из-за малой прозрачности или окрашенности среды, очень малой концентрации или других причин. [2]
Потенциометрическое определение рН водных растворов является надежным методом, дает истинное значение ( - ( в растворе. [3]
Потенциометрические определения основаны на том, что потенциал ряда электродов является функцией активностей компонентов соответствующих окислительно-восстановительных систем. [4]
 |
Гальванический элемент, состоящий из стеклянного и хлорсеребряного электродов. [5] |
Потенциометрические определения основаны на том, что потенциал электродов является функцией концентраций ( активностей) соответствующих потенциалопределяющих ионов. [6]
Потенциометрические определения рН получили широкое распространение благодаря высокой точности определения, которую они могут дать, и применимости их к сложным системам, для которых колориметрические и другие методы не могут дать удовлетворительных результатов из-за малой прозрачности ( или окрашенности) среды, очень малой концентрации или по другим причинам. [7]
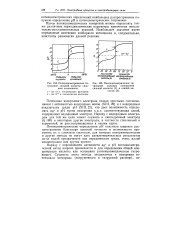 |
Потенциометрическое титрование сильной кислоты сильным основанием.| Потенциометрическое титрование сильным основанием сильной кислоты ( / и слабой кислоты ( 2. [8] |
Потенциометрические определения рН получили широкое распространение благодаря высокой точности и возможности применять их к сложным системам, для которых колориметрические и другие методы не могут дать удовлетворительных результатов из-за малой прозрачности или окрашенности среды, очень малой концентрации или других причин. [9]
Потенциометрическое определение не только смеси кислот или оснований с близкими константами диссоциации, но и смеси ряда сильных кислот успешно можно осуществить в неводных растворах благодаря дифференцирующим свойствам различных органических растворителей ( см. гл. [10]
Потенциометрические определения рН являются настолько обычными, что нет необходимости останавливаться на них детально. Однако следует упомянуть об использовании стеклянного электрода в химии крови. Особенно стоит отметить, что для этих измерений требуется незначительное количество образца. [11]
Потенциометрические определения рН получили широкое распространение благодаря высокой точности и возможности применять их к сложным системам, для которых колориметрические и другие методы не могут дать удовлетворительных результатов из-за малой прозрачности или окрашенности среды, очень малой концентрации или других причин. [12]
 |
Сосуд для потенциометричес-кого титрования.| Каломельный электрод. [13] |
Потенциометрические определения [8, 106] выполняют также в сосудах ( рис. 115), изготовляемых из капилляров диаметром 1 - 2 мм. В сосуд впаяна - платиновая проволока 2, служащая электродом и соединенная медной проволокой 4 через ртутный контакт 3 с потенциометром. [14]
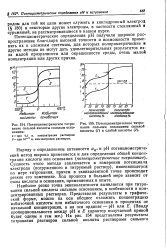 |
Потенциометрическое титро - [ IMAGE ] Потенциометрическое титрование сильной кислоты сильным осно - вание сильным основанием Сильной ванием. кислоты ( / и слабой кислоты ( 2. [15] |
Страницы: 1 2 3 4