Фенильный остаток
Cтраница 1
Фенильный остаток, активированный эфирной группой, выступает при этом в качестве нуклеофильного агента. Аллильные эфиры, замещенные в у-положении, дают а-замещенные аллилфенолы. [1]
Фенильный остаток в бифениле действует как электроноакцепторная группа и эффективно стабилизует промежуточный карбанион в бензильиом положении. Ранние литературные данные по восстановлению би-фенила в различных условиях реакции были противоречивы. Среди продуктов были обнаружены 1 4 - и 3 4-дигидробифенил, а в более жестких условиях - тетра - и гексагидробифенилы. Дианион, генерированный при - 75 С, дает 1 4-дигидробифенил [105]; совершенно очевидно, что быстрое восстановление и осторожная обработка приводят к ожидаемым результатам. [2]
Фенильный остаток, активированный эфирной группой, выступает при этом в качестве нуклеофильного агента. Аллильные эфиры, замещенные в Y-положении, дают а-замещенные аллилфенолы. [3]
Фенильный остаток барбана при метаболизме не гидро-ксилируется. [4]
Возможность миграции фенильного остатка или цепи этиламина предопределяет два альтернативных пути реакции. Ион LXXXII, постулируемый как промежуточный продукт реакции [ 286, ср. [5]
При введении третьего фенильного остатка в молекулу дифенил-метанового красителя цвет несколько углубляется, так как хромофорная система красителя расширяется. Например, замещение атома водорода при центральном атоме углерода в гидроле Михлера фенильным остатком приводит к сдвигу максимума поглощения от 603 5 до 621 нм. Цвет красителя при этом должен быть голубым. Но поскольку при таком замещении возникает конкурирующая сопряженная цепочка, в которой также происходят электронные переходы, то появляется второй максимум поглощения, соответствующий дополнительному желтому цвету. [6]
Этот механизм подтверждается наличием фенильного остатка катализатора в качестве концевой группы полимера. [8]
При введении заместителя в третий фенильный остаток в орто-положение к центральному атому углерода цвет красителя повышается, так как при этом этот фенильный остаток выходит из плоскости двух других бензольных колец, что ведет к разобщению системы сопряжения. [9]
Несмотря на то, что положение фенильного остатка в пиридиновом кольце не установлено, по аналогии с характером замещения в реакции Гомберга, можно полагать, что замещение происходит в положение 4 пиридинового кольца. [10]
Несмотря на то, что положение фенильного остатка в пиридиновом кольце не установлено, по аналогии с характером замещения в реакции Гомберга, можно полагать, что замещение происходит в положение 4 пиридинового кольца. [11]
Сравнительно объемистые метильные группы ( и еще более громоздкий фенильный остаток) оставляют лишь очень небольшое число возможностей для приближения нуклеофильного реагента, и переходное состояние обладает большей степенью упорядоченности, чем исходное состояние, поэтому энтропия активации должна стать более отрицательной. Кроме того, из-за пространственных препятствий ( и индуктивного эффекта алкильных групп) снижается степень перекрывания между нуклеофильным реагентом и центральным атомом углерода в переходном состоянии, которое, таким образом, обладает более высокой энергией. Отсюда следует более высокая энергия активации для соответствующей реакции. [12]
Из приведенных данных следует, что влияние фенильного остатка больше, чем одной метильной группы, но меньше, чем двух метальных групп. Хотя углеродный атом, соединенный с фенилом, несет некоторый положительный заряд в переходном состоянии, но вряд ли его можно представить в виде открытого карбониевого иона. [13]
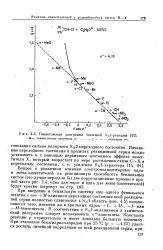 |
Гамлетовская диаграмма типичной 8м1 - реакции. [14] |
При введении в бензильную систему еще одного фенильного остатка с его 71 / - влиянием переходные состояния всей реакционной серии полностью сдвигаются в 8к1 - область ( рис. 4.5) независимо от того, имеются ли в арильных ядрах / -, - Л / -, - 7 - или - М - заместители. В соответствии с 8к1 - механизмом в гамметов-ской диаграмме следует использовать о - константы. Константа реакции р отрицательна и имеет довольно большую величину. [15]
Страницы: 1 2 3 4