Количество пероксидазы
Cтраница 1
Количество пероксидазы, протеазы и амилазы возрастает в смесях под влиянием автолитических процессов даже в отсутствии кислорода. [1]
Количество пероксидазы, протеазы и амилазы возрастает при двухдневном стоянии намоченной муки ростков пшеницы даже в отсутствии кислорода под влиянием автолитических процессов. [2]
Количество пероксидазы возрастает с той же закономерностью, как и интенсивность дыхания. Однако, когда интенсивность дыхания начинает падать, количество пероксидазы продолжает возрастать. [3]
Увеличение количества пероксидазы и амилазы в растворе клейковины, переваренной трипсином, под влиянием окисления превышает в благоприятных условиях 100 % первоначального содержания этих ферментов. [4]
Как видно, количество образовавшегося пурпурогалина всегда пропорционально количеству пероксидазы - перекиси водорода при условии, если пирогаллол имеется в достаточном количестве. [5]
Если действовать равными количествами перекиси водорода на пирогаллол в присутствии возрастающих количеств пероксидазы и взвешивать образующийся пур-пурогалин, то оказывается, что выше определенной границы дальнейшее прибавление пероксидазы не оказывает никакого влияния на количество реагирующего вещества. Аналогичная граница наблюдается также и для перекиси водорода, если применять постоянные количества пероксидазы и возрастающие количества перекиси водорода. Количество прореагировавшего вещества прямо пропорционально количеству перекиси водорода при избытке пероксидазы и количеству пероксидазы при избытке перекиси водорода. [6]
Увеличение количества выделяющегося иода, вызванное перокси-дазой, не прямо пропорционально количеству пероксидазы, как это имеет место при окислении пирогаллола, а растет медленнее, чем последнее. [7]
В зоне ткани, включающей камбий, не было отмечено периферических изменений в количестве пероксидазы. [8]
Серии опытов были расположены по возрастающим концентрациям пероксидазы таким образом, чтобы в каждой серии реакционные колбочки содержали постоянное количество пероксидазы и возрастающие количества иодистоводородной кислоты. [9]
Если сравнить эти количества с количеством перекиси водорода, которое может быть активировано данной пероксидазой, то оказывается, что количество пероксидазы, необходимое для активирования 1 молекулы перекиси водорода, полностью уничтожается 2 молекулами солянокислого гидроксиламина и цианистого калия и х / 4 молекулы сульфата гидразина. Для более точного суждения об этих отношениях необходимо поставить дальнейшие опыты с целью выяснения действия кислот и щелочей на пе-роксидазу. [10]
Бах и Шода2 исследовали количественно действие пероксидазы при окислении пирогаллола посредством перекиси водорода, определяя образующийся пурпурогалин, и установили, что при постоянном и избыточном количестве перекиси водорода выход пурпуро-галипа пропорционален количеству пероксидазы, а при постоянном избытке пероксидазы - количеству перекиси водорода. Эта пропорциональность наблюдается только до определенного предела, после которого дальнейшее прибавление пероксидазы или, соответственно, перекиси водорода не вызывает увеличения количества пурпурогалина. Этот предел соответствует, следовательно, полному использованию субстрата и указывает на максимальный выход пурпурогалина. Выходы, полученные Бахом и Шода в шести опытах, колеблются между 16.2 и 16.8 % и приближаются к максимальным выходам Ниренштейна и Спирса. Он считает, что Бах и Щода получили значительно меньшие выходы потому, что они применяли слишком большие концентрации перекиси водорода и работали с менее чистой пероксидазой. Учитывая эти данные, мне казалось небезинтересным проверить активность очищенной путем ультрафильтрования пероксидазы ( см. предшествующую статью) при окислении пирогаллола перекисью водорода. [11]
Для проведения исследования о распределении перекиси водорода между субстратом и ферментами было далее необходимо определить скорость реакции, вызываемой приготовленным мною препаратом каталазы, так как только при точном знании этой скорости можно применять сравнимые количества пероксидазы и каталазы. Обычный метод, применявшийся также и Сентером8 в его основном исследовании о скорости реакции каталазы, неприменим в условиях моих опытов. Оказалось, что при отборе проб жидкости пипеткой из реакционной склянки внутри пипетки происходит такое энергичное выделение кислорода, что точное измерение объема жидкости практически невозможно. [12]
Комплекс II образуется из эквимолекулярных количеств пероксидазы и перекиси водорода, а при избытке перекиси он переходит в комплекс III. Оба эти комплекса быстро реагируют с донорами водорода. Окись углерода не влияет на их спектр, что привело Кейлина и Манна [46] к предположению о трехвалентном состоянии атома железа. Позже, в 1942 г. Теорелл [20, 47] наблюдал, что бледно-красный комплекс II образуется не сразу после добавления пероксидазы к перекиси водорода и что вначале получается нестойкий окрашенный в зеленый цвет комплекс, который очень быстро превращается в бледнокрасный комплекс II. [13]
Контрольные опыты с прибавленными заранее ничтожными количествами пероксидазы показали, что раствор совершенно не содержит задерживающих веществ. Аналогичный опыт, поставленный с зимином, дал такие же результаты. [14]
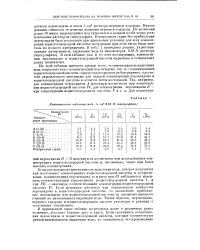 |
Интенсивность выделения иода ( в см3 N гипосульфита. [15] |
Страницы: 1 2 3