Присоединение - молекулярный кислород
Cтраница 1
Присоединение молекулярного кислорода имеет мало значения в лабораторной практике. [1]
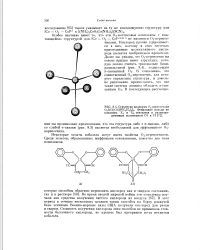 |
Структура молекулы О2 - переносчика. [2] |
Кислород прочно удерживается в них, поэтому в этих системах присоединение молекулярного кислорода является необратимым процессом. [3]
Бах еще в 1897 г. предположил, что при окислении происходит присоединение молекулярного кислорода с образованием перекиси, которая может впоследствии разлагаться и передавать свой кислород другим молекулам. [4]
Для механизма дальнейших стадий автоокисления углеводородов важной является установленная на примере трифенилметила легкость присоединения молекулярного кислорода к свободным углеводородным радикалам. И хотя данные о способности других, вчаст-ности высокомолекулярных и низших, алифатических, радикалов реагировать с кислородом пока отсутствуют, можно полагать, что и эти радикалы ведут себя аналогичным образом. [5]
Не менее сильное влияние, по-видимому, оказывают антиокси-данты на аэробные трансэлектроназы - ферменты, активирующие присоединение молекулярного кислорода. Наиболее же чувствительное звено к действию антиоксидантов, как показали опыты этих авторов, находится в оксидазной системе между цитохромом и цитохромоксидазон. [6]
Одним из преимуществ является и улучшенный вариант эффекта Хальдана [668, 669], который заключается в освобождении протонов при присоединении молекулярного кислорода к гемоглобину, и наоборот. Этот эффект важен для транспорта молекулярного кислорода из легких к потребляющим кислород тканям, а также для транспорта протонов из этих тканей к легким. Большое значение имеет также возможность использования некоторых специальных органических фос-форильных соединений, таких, как 2 3-дифосфоглицерат ( ДФГ); или инозитолгексафссфат [670, 671], в качестве аллостерических эффекторов, благоприятствующихдезоксиконформации. [7]
Таким образом, активирование кислорода при процессах медленного окисления обусловливается пе расщеплением нейтрального кислорода на озон и аитозон, как это принимал Шенбейн, не присоединением молекулярного кислорода к водороду воды, как это принимал Траубе, а первичным, прямым образованием перекисей путем присоединения молекулярного кислорода к окисляемому веществу. [8]
Таким образом, активирование кислорода при процессах медленного окисления обусловливается пе расщеплением нейтрального кислорода на озон и аитозон, как это принимал Шенбейн, не присоединением молекулярного кислорода к водороду воды, как это принимал Траубе, а первичным, прямым образованием перекисей путем присоединения молекулярного кислорода к окисляемому веществу. [9]
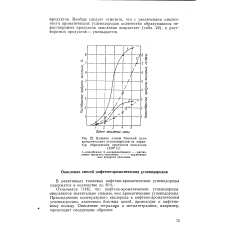 |
Влияние длины боковой цепи ароматических углеводородов на характер образующих продуктов окисления. [10] |
Отмечается [ 1461, что нафтено-ароматические углеводороды, окисляются значительно сильнее, чем ароматические углеводороды. Присоединение молекулярного кислорода к нафтено-ароматическим углеводородам, лишенным боковых цепей, происходит к нафтеновому кольцу. [11]
В растениях имеется фермент липоксигеназа. Он катализирует присоединение молекулярного кислорода к линолевой, линолено-вой и арахидоновой кислотам1 в результате, образуются перокси-ды этих кислот. Установлено, что пероксиды в гомогенатах растений способны окислять некоторые фенольные вещества, как, например, нордигидрогваяретовую кислоту, пирокатехин, гидрохинон. [12]
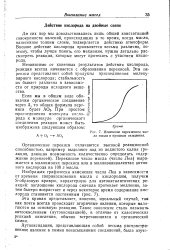 |
Изменение перекисного чис-ла масла в процессе окисления. [13] |
Независимо от конечных результатов действия кислорода, реакция всегда начинается с образования перекисей. Эти перекиси представляют собой продукты присоединения молекулярного кислорода; стабильность их бывает различна в зависимости от природы исходного веще-ства. [14]
Аутоксидацией называется инициированное свободными радикалами медленное окисление органических соединений кислородом воздуха. Реакция начинается благодаря способности свободных радикалов к присоединению молекулярного кислорода. [15]
Страницы: 1 2