Произведение - растворимость - вещество
Cтраница 1
Произведение растворимости вещества А, Ап, распадающегося в воде на ионы по уравнению: К. [1]
 |
Произведения растворимости труднорастворимых веществ. [2] |
По произведению растворимости вещества можно легко рассчитать его растворимость в чистой воде, не содержащей каких-либо других веществ. [3]
Зная величину произведения растворимости вещества, можно приблизительно подсчитать, насколько понизится растворимость его от прибавления электролита с одноименным номом. [4]
 |
Характеристика качества воды рек СССР. [5] |
Зная величину произведения растворимости вещества, нетрудно определить и его общую предельную растворимость. [6]
Что называется произведением растворимости вещества. [7]
Коэффициент распределения зависит от соотношения произведений растворимости соосаждающихся веществ. Чем больше разница в растворимостях, тем меньшее количество более растворимого компонента содержит осадок менее растворимого вещества. Если произведения растворимости различаются в 103 - 104 раз, то практически можно в равновесных условиях получить чистые твердые фазы даже при наличии изоморфизма между двумя солями, находящимися в растворе. [8]
Коэффициент распределения зависит от соотношения произведений растворимости соосаждающихся веществ. Чем больше разница в растворимостях, тем меньшее количество более растворимого компонента содержит осадок менее растворимого вещества. Если произведения растворимости отличаются в 103 - 104 раз, то практически можно в равновесных условиях получить чистые твердые фазы даже при наличии изоморфизма между двумя солями, находящимися в растворе. [9]
Коэффициент распределения зависит от соотношения произведений растворимости соосаждающихся веществ. Чем больше разница в растворимостях, тем меньшее количество более растворимого компонента содержит осадок менее растворимого вещества. Если произведения растворимости различаются в 103 - 104 раз, то практически можно в равновесных условиях получить чистые твердые фазы даже при наличии изоморфизма между двумя солями, находящимися в растворе. [10]
Коэфициент распределения зависит от соотношения произведений растворимости соосаждающихся веществ. Чем больше разница в растворимостях, тем меньшее количество более растворимого компонента содержит осадок менее растворимого вещества. Если произведения растворимости отличаются в 103 - 104 раз, то практически можно в равновесных условиях получить чистые твердые фазы, несмотря на наличие изоморфизма между двумя солями, находящимися в растворе. [11]
А в чистой воде; 2) произведение растворимости вещества А, приняв, что коэффициенты активности ионов у 1 ( растворы сильно разбавлены); 3) растворимость вещества А в растворе, содержащем 0 01 моль вещества В; 4) растворимость вещества А II растворе, содержащем 0 01 моль вещества С. Вещества А, В, С полностью диссоциированы. [12]
В ] [ А - ] превышает произведение растворимости S вещества ВА, то соответствующая часть этой соли выпадает в осадок. Таким образом, может произойти осаждение до достижения точки эквивалентности. Это происходит, например, при образовании комплекса HgJ4 - - ( см. стр. [13]
Произведение двух констант Кс [ МА ( К ] обозначают символом ПР и называют произведением растворимости вещества МА. [14]
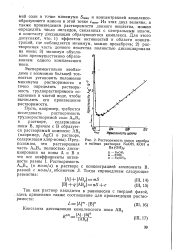 |
Растворимость окиси серебра. [15] |
Страницы: 1 2