Процесс - образование - аммиак
Cтраница 1
Процесс образования аммиака, как видно из уравнения, обратим, экзотермичен и протекает с уменьшением объема. Согласно существующему принципу равновесие должно смещаться вправо с понижением температуры и с увеличением давления. Но при низких температурах, как известно, скорость реакции незначительная, она повышается только при высокой температуре и в присутствии катализатора. [1]
Процесс образования аммиака, как видно из уравнения, обратим, экзотермичен и протекает с уменьшением объема. Согласно принципу Ле Шателье ( стр. Но при низких температурах, как известно, скорость реакции незначительная, она повышается только при высокой температуре и в присутствии катализатора. Поэтому в промышленности синтез аммиака ведут при 450 - 525 С и под давлением 300 атм. [2]
Процесс образования аммиака из водорода и азота проводим следующим образом. Количества газов в резервуарах так велики, что уменьшение их на несколько молей не изменяет давлений в резервуарах. [3]
Катализаторами процесса образования аммиака из азота и водорода являются многие металлы. Промышленное применение получили катализаторы на основе железа - наиболее активные и дешевые по сравнению с другими. [4]
Если бы процесс образования аммиака проходил количественно ( а это невозможно вследствие обратимости реакции), то из 1000 м3 стехиометрической смеси азота и водорода было бы получено 500 м3 аммиака. [5]
Катализаторами, ускоряющими процесс образования аммиака, являются железо, осмий, уран, молибден, марганец, вольфрам и некоторые другие металлы. [6]
Из того, что для процесса образования аммиака из азота и водорода АОбтз 5 8 ккал / моль, можно лишь сделать вывод, что синтез аммиака при 400 С неосуществим, если каждый из реагентов находится под атмосферным давлением. Но считать, что этот процесс при 400 С вообще невозможен, было бы ошибочным. Действительно, при высоких давлениях синтез аммиака становится возможным. [7]
Из того, что для процесса образования аммиака из азота и водорода АСЦ73 24 кДж, можно лишь сделать вывод, что синтез аммиака при 400 С неосуществим, если каждый из реагентов находится под атмосферным давлением. Но считать, что этот процесс при 400 С вообще невозможен, было бы ошибоч-вым. Действительно, при высоких давлениях синтез аммиака становится воз-ножным. [8]
На основании того, что для процесса образования аммиака из азота и водорода Ас тз 24 кДж, можно лишь сделать вывод, что синтез аммиака при 400 С неосуществим, если каждый из реагентов находится под атмосферным давлением. Но считать, что этот процесс при 400 С вообще невозможен, было бы ошибочным. Действительно, при высоких давлениях синтез аммиака становится возможным. [9]
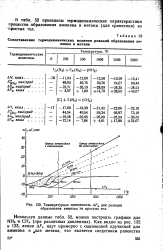 |
Температурная зависимость AFH для реакции образования аммиака из простых тел. [10] |
В табл. 52 приведены термодинамические характеристики процессов образования аммиака и метана ( для сравнения) из 4 простых тел. [11]
Из этих исследований вытекает, что на открытых площадях нитрификация берет верх над процессом образования аммиака, под пологом же леса аммиак накопляется в больших количествах. [12]
 |
Колонна синтеза аммиака с полочной насадкой.| Колонна синтеза аммиака с двойными тешюотводящими трубками. [13] |
Электроподогреватель мощностью 1100 кВт, размещенный в центральной трубе катализаторной коробки, предназначен для разогрева и восстановления катализатора, а также для поднятия температуры до начала процесса образования аммиака после остановок агрегата. Теплообменник расположен под катализаторной коробкой. [14]
Таким образом, исследованиями многих химиков, произведенными до 1913 года и теми, которые были произведены до сих пор установлено, что 1) реакция образования аммиака протекает весьма медленно при низких температурах, 2) высокие температуры ( выше 400) способствуют ускорению распада молекулы ам миака, 3) катализаторы действуют ускоряюще на процесс образования аммиака, и лучшие винходы его получаются тогда, когда реагирующие газы находятся под высоким давлением. [15]
Страницы: 1 2