Разбавление - метан
Cтраница 2
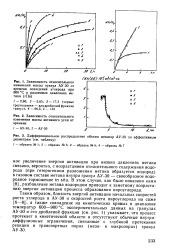
Как видно из рис. 6, а, выходы формальдегида растут с увеличением разбавления метана воздухом. [16]
По-видимому, приведенное соотношение исходной газовой смеси, подвергающейся пиролизу, не является оптимальным, так как при разбавлении метана хлором возможны более высокие концентрации ацетилена в отмытых от хлористого водорода газах термоокислительного пиролиза метана. [17]
Итак, высокая температура ( 1500 - 1800 С), пониженное парциальное давление метана ( понижение общего давления ниже атмосферного или разбавление метана водородом, инертным газом), кратковременное пребывание газа в зоне реакции - таковы оптимальные условия получения ацетилена из метана. [18]
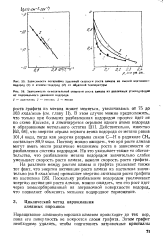
На эффективность разряда в отношении превращения углеводородов может влиять и изменение других условий. При четырехкратном разбавлении метана аргоном ( при pcnt 10 мм рт. ст.) ф увеличивается приблизительно в 8 раз ( от 0 5 до 3 9), при дальнейшем разбавлении ф практически не изменяется. При разбавлении водородом в аналогичных условиях ф, если и увеличивается, то лишь очень незначительно. [19]
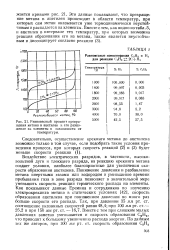 |
Равновесный процент превращения метана в ацетилен и его разложение на элементы в зависимости от температуры. [20] |
Воздействие электрических разрядов, в частности, высоковольтной дуги и тлеющего разряда, на реакцию крекинга метана создает условия, наиболее благоприятные для увеличения скорости образования ацетилена. Понижение давления и разбавление метана инертными газами или водородом и уменьшение времени пребывания газа в зоне разряда позволяет в значительной мере уменьшить скорость реакции термического распада на элементы. Как показывают данные Еремина и сотрудников по изучению электрокрекинга метана в статических условиях [42], скорость образования ацетилена при пониженном давлении во много раз больше скорости его распада. Вместе с тем при слишком малых давлениях заметно уменьшается и скорость образования С2Н2, что приводит к большому увеличению расхода энергии. [21]
Разность скоростей реакций образования и разложения метана зависит и от давления, так как процесс термоокислительного пиролиза метана протекает с увеличением объема получаемых газов. Поэтому понижение давления или разбавление метана инертными газами способствуют сдвигу реакции в сторону образования ацетилена. [22]
В этом случае, как было показано нами [8], разбавление метана водородом приводит к заметному возрастанию энергии активации процесса образования пироуглерода. [24]
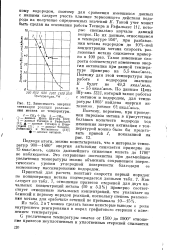 |
Зависимость энергии активации реанции разложения метана от температуры. [25] |
Такой учет может быть сделан на основании работы Теснера и Рафалькес [1], которые специально изучали данный вопрос. По их данным, относящимся к температуре 950, при разбавлении метана водородом до 10 % - ной концентрации метана скорость разложения метана снижается примерно в 100 раз. Такое изменение скорости соответствует изменению энергии активации при данной температуре примерно на 5 5 ккал / молъ, Поэтому для этой температуры при работе с водородом значение Е будет не 49 3 ккал / молъ, а - 55 ккал / молъ. [26]
При соотношении между фтором и азотом 2: 1 и разбавлении метана азотом в пять раз, что соответствует молярному соотношению между фтором, метаном и азотом в реакционной смеси 2: 1: 10, количество продуктов, кипящих выше, чем четырехфтористый углерод, составляет 45 % ( объемн. Поэтому они могут быть выделены вымораживанием из нижних слоев смеси с последующей отгонкой жидкости. Эта работа ясно указывает на то, что процесс прямого фторирования может привести к образованию углеродной цепи за счет полимеризации. [27]
В-третьих, в работе [38] указывается, что при термическом разложении метилтрихлорсилана выход, карбида кремния значительно повышается при замене инертного газа-носителя гелия на водород. При этом также подавляется образование свободного углерода ( сажи) в объеме. Действительно, известно, что разбавление метана гелием существенно повышает скорость объемной реакции разложения метана, что ведет к образованию сажи. Когда же добавляется водород, скорость гетерогенной реакции роста графита увеличивается, что и влечет за собой увеличение скорости роста карбида кремния. [28]
Скорость горения водорода превышает скорость горения углеводородов. Следовательно, при добавлении водорода к метано-кис-лородной смеси необходимый для процесса высокий температурный уровень может быть достигнут частично и за счет сгорания водорода. Поэтому были основания ожидать, что с разбавлением метана водородом значение полезного крекинга должно возрасти. В работе Фишера и Пихлера3, проведенной на небольшой лабораторной установке, термоокислительному пиролизу был подвергнут коксовый газ. Максимальное значение полезного крекинга, равное 50 %, было получено в условиях внешнего нагрева реакционной зоны до 1600 С и времени пребывания тФ 002 сек. [29]
Страницы: 1 2 3