Разложение - перекисное соединение
Cтраница 1
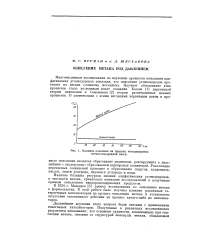 |
Влияние давления на пределы воспламенения метано-водородной смеси. [1] |
Разложение перекисных соединений приводит к образованию спиртов, альдегидов, кислот, окиси углерода, двуокиси углерода и воды. [2]
 |
Пределы воспламенения некоторых смесей газов. [3] |
Разложение перекисных соединений происходит в присутствии некоторых металлов ( железа, меди, марганца, кобальта, хрома) и их солей, являющихся катализаторами. Поэтому концентрированная перекись водорода, надуксусная кислота, а также ряд других перекисей способны взрываться в отсутствие органических веществ. [4]
Продукты разложения перекисных соединений метилциклогексанонов моно - и дикарбоновые кислоты ( Рх) - включаются в координационные сферы комплексов 2ROOH - MeSt2 с образованием смешанных комплексов. [5]
Раствор формалина применяется для разложений перекисных соединений. Добавлять его следует осторожно при размешивании. [6]
Для предупреждения подобных аварий, связанных с разложением перекисных соединений, следует особое внимание уделять строгому соблюдению заданного технологического режима. Технологические процессы, в которых участвуют концентрированные перекиси, должны быть максимально автоматизированы и оснащены надежными блокировками, обеспечивающими безопасную остановку производства при аварийных ситуациях или нарушениях нормального технологического режима. [7]
Аппараты перед чисткой следует промывать горячей водой для разложения перекисных соединений, накопление которых вместе с осадком полимера на практике наблюдалось неоднократно. [8]
По нашему мнению, влияние природы растворителя на скорость разложения перекисных соединений может проявляться не только через индуцированное ее разложение, но и непосредственно в результате бимолекулярной реакции перекиси или гидроперекиси с растворителем. Как нам кажется, такое предположение довольно убедительно подтверждается результатами наших экспериментов. [9]
Второй член правой части уравнения ( 3) соответствует скорости разложения перекисных соединений на стенках сосуда и на электродах, в объеме раствора, а также возможного окисления и восстановления НОГ на аноде и катоде. [10]
Грей и Вильяме [61] также приводят таблицы по энергиям активации разложения перекисных соединений. [11]
Во всех цитированных выше работах влияние природы растворителя на скорость разложения перекисных соединений считается обусловленным индуцированным их разложением. Если реакцию проводить в условиях, исключающих индуцированное разложение перекисных соединений, то, как было показано в работах [20, 21], скорость реакции очень мало зависит от природы растворителя. [12]
В патентной литературе [38] предлагается использовать соединения такого типа для предотвращения разложения перекисных соединений. [13]
Таким образом, реакции металлоорганпческпх соединений с кислородом должны рассматриваться во взаимной связи с образованием и разложением металлоорганиче-ских перекисных соединений. [14]
Таким образом обусловливаемые кислородом невоспроизводимость условий полимеризации, изменение параметров процесса в ходе полимеризации, взаимодействие растущих цепей с продуктами разложения перекисных соединений являются причиной получения ПВХ, неоднородного по своим химическим и физическим характеристикам, в связи с чем резко ухудшается его перерабатываемость. [15]
Страницы: 1 2