Расчет - равновесие
Cтраница 1
Расчеты равновесия показывают, что для достижения в конвертированном газе достаточно низкой концентрации окиси углерода конверсию следует вести при температуре не выше 250 С. [1]
 |
Метод расчета, предложенный М. П. Сусаревым и А. Н. Горбуновым. [2] |
Расчет равновесия между жидкостью и паром по этому методу сводится к следующим операциям. [3]
Расчеты равновесия и материального баланса выполняются аналогичным образом поочередно до четвертой тарелки снизу. [4]
Расчет равновесия жидкость - пар в системе водород - метан - этилен в диапазоне температур 123 - 248 К и давлений 0 1 - 3 0 МПа. [5]
Расчет равновесий по этому уравнению подробно рассматривается в главе VI Справочника ( см. выпуск второй, стр. [6]
Расчет равновесий по этому методу представляет собой математически довольно сложную задачу. [7]
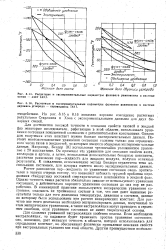 |
Расчетные и экспериментальные параметры фазового равновесия в системе метан - азот.| Расчетные и экспериментальные параметры фазового равновесия в системе двуокись углерода - сероводород. [8] |
Расчет равновесия пар-жидкость по уравнению состояния очень притягателен в первую очередь потому, что позволяет избежать трудной проблемы определения стандартных состояний сверхкритических компонентов в жидкой фазе. Однако точность таких расчетов обязательно зависит от используемого уравнения состояния, а действительно хорошего уравнения состояния до сих пор не разработано. В инженерной практике используются эмпирические уравнения состояния; опасность их применения состоит в том, что они дают надежные результаты только для того диапазона темпер. Для расчетов вне этого диапазона необходимо экстраполировать данные, полученные по этим эмпирическим уравнениям, а такие экстраполяции могут приводить к серьезным ошибкам, если уравнение состояния не имеет теоретической основы. [9]
Расчет равновесия с участием комплексов представляет часто более трудную задачу, чем подобный же расчет для многоосновных кислот, из-за присутствия в заметных концентрациях нескольких разнотипных частиц. Однако, если известен рН кислотно-основной системы, то легко произвести расчет концентраций и всех остальных существующих в растворе частиц; точно также, если известна концентрация лиганда, то для одноядерного комплекса легко рассчитать и концентрации всех остальных частиц в растворе. Как будет видно из последующих примеров, графические методы, используемые для кислотно-основных систем, применимы и к системам, содержащим комплексы. [10]
 |
Метод расчета фазового равновесия в тройной системе, предложенный Сусаревым и Горбуновым. [11] |
Расчет равновесия между жидкостью и паром по этому методу состоит из следующих операций. [12]
Расчет равновесия заключается н нахождении с помощью приведенных уравнений коэффициентов активности, по значениям которых по уравнениям ( 58) или ( 62) определяются составы равновесных фаз. [13]
Расчет равновесий необходим при рассмотрении особенностей кривых титрования с целью правильного выбора индикатора. [14]
Расчет равновесия заключается в нахождении с помощью приведенных уравнений коэффициентов активности, по значениям которых по уравнениям ( 58) или ( 62) определяются составы равновесных фаз. [15]
Страницы: 1 2 3 4