Расчет - энтропия
Cтраница 1
Расчет энтропии существенно упрощается, если речь идет об идеальном газе. [1]
Расчет энтропии осуществляется для стандартных условий по формуле, которую легко получить следующим способом. [2]
Расчет энтропии основывается на определении теплоемкости при разных температурах. Количество поглощаемой телом теплоты равняется произведению его теплоемкости на повышение температуры. [3]
Расчет энтропии осуществляется для стандартных условий по формуле, которую легко получить следующим способом. [4]
Расчеты энтропии показывают, что подвижность адсорбированного H2S сильно ограниченна. [5]
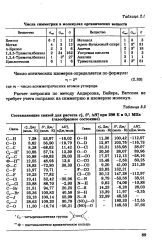 |
Числа симметрия в молекулах органических веществ. [6] |
Расчет энтропии по методу Андерсона, Байера, Ватсона не требует учета поправок на симметрию и изомерию молекул. [7]
Расчет энтропии при 16 К по данным [1322] приводит к величине Sie 0 0040 кал / г-атом - град, в то время как в работе [1320] при определении 5298 is использовалось более высокое значение 516 0.006 2 кал / г-атом - град. [8]
Расчеты энтропии активации могут оказать существенную пользу для суждения о конфигурации переходного состояния. [9]
Расчеты энтропии смешения, описанные выше в общих чертах, содержат в скрытом виде предположение, что теплота смешения обоих сортов молекул равна нулю. Если это не верно, то различные конфигурации будут энергетически неравноценны и, следовательно, не одинаково вероятны. Таким образом, при рассмотрении реальной смеси, мы должны пересмотреть этот расчет с учетом влияния теплоты смешения на неупорядоченность процесса смешения. [10]
Расчет энтропии MgO при 298 15 К поданным [ 3192, 1711 и 640 ] приводит к величинам 6 4 0 1; 6 66 0 02 и 6 43 0 05 кал / моль - град, соответственно. [11]
Расчет энтропии раствора ведется при допущении, что сумма вкладов поступательного, колебательного и вращательного движений остается без изменений при смешении. [12]
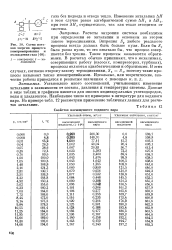 |
Схема потоков энергии процесса компримирования и охлаждения газа. [13] |
Расчеты энтропии системы необходимы при определении ее энтальпии и основаны на втором законе термодинамики. Энтропия Sp любого реального процесса всегда должна быть больше нуля. Если бы Sp была равна нулю, то это означало бы, что процесс совершается без трения. Такие процессы называются обратимыми. В расчетах обычно принимают, что в механизмах, совершающих работу ( насосах, компрессорах, турбинах), процессы являются адиабатическими и обратимыми. [14]
Расчет энтропии алканов ( парафинов) изостроения по Эвеллу проводился на базе эшропии нормальных углеводородов, рассчитанной по уравнению ( 101) и установленным ( см. ниже правилам Эвелла. [15]
Страницы: 1 2 3 4