Тримолекулярная реакция
Cтраница 1
Тримолекулярная реакция является реакцией третьего порядка, когда ее скорость пропорциональна произведению концентраций трех реагентов. [1]
Тримолекулярная реакция [ уравнение ( 26) ] менее вероятна, чем реакции, описанные уравнениями ( 25) и ( 27), в которых образование я-комплекса или комплекса электрофильного реагента с X предшествует стадии, определяющей скорость процесса. [2]
Тримолекулярные реакции представляют собой реакции, которые требуют участия трех индивидуальных частиц в элементарном процессе. [3]
Тримолекулярные реакции практически встречаются очень редко; наиболее частыми и преимущественными в производственной практике являются бимолекулярные реакции. [4]
Тримолекулярные реакции могут, вообще говоря, требовать энергии активации, хотя в случае реакций ассоциации типа реакции (1.6) энергия активации, вероятно, очень мала. [5]
Тримолекулярные реакции встречаются очень редко. [6]
Тримолекулярные реакции, при которых сталкиваются и взаимодействуют три молекулы, встречаются сравнительно редко; обычно они идут постадийно. [7]
Тримолекулярные реакции возникают значительно реже бимолекулярных и в полупроводниковой технике менее важны. На рис. VI.2 показан ход мономолекулярной, бимолекулярной и тримолекулярной реакций в координатах С f ( t), где С - концентрация исходного вещества, убывающая в процессе реакции. Из рисунка видно, что быстрее всех протекают мономолекулярные реакции. [8]
Тримолекулярная реакция протекает с участием трех частиц при их одновременном столкновении. Иногда бимолекулярное превращение происходит с участием третьей частицы. [9]
Тримолекулярные реакции представляют собой реакции, которые требуют участия трех индивидуальных частиц в элементарном процессе. [10]
Тримолекулярные реакции, в которых принимает участие одна молекула растворителя, вполне возможны. Если мы выделим из этого механизма бимолекулярную лимитирующую стадию переноса протона, происходящую при быстром захвате воды, то получим обратное доказательство справедливости общего механизма катализируемой кислотами дегидратации ( стр. [11]
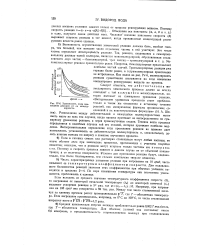 |
Зависимость хода про - J. [12] |
Тримолекулярные реакции уже гораздо более редки, а тетрамолекулярные практически не встречаются. Как видно из рис. IV-6, молекулярность реакции существенно сказывается на ходе изменения концентрации реагирующих веществ во времени. [13]
Тримолекулярные реакции встречаются реже ( например, 2NO Н2 N2O H2O), так как одновременное столкновение трех молекул маловероятно. Реакции более высоких значений молекулярности не встречаются. [14]
Тримолекулярные реакции встречаются реже ( например, 2NO H2 N20 H20), так кяк одновременное столкновение трех молекул маловероятно. Реакции более высоких значений молекулярное не встречаются. [15]
Страницы: 1 2 3 4