Сиджвик
Cтраница 1
Сиджвик [14] приписывает Слейтсру [32] сообщение о том, что метил - и этшшитриты реагируют быстрее амилнитрита. Хотя в статье Слейтсра об этом ire говорится и не приводится экспериментальных данных, относящихся к этому вопросу, вероятно, является правильным предположение, согласно которому низшие, гомологи обладают большей реакционной способностью. Повидимому, наиболее важное преимущество применения газообразных алкилнитритов состоит п том, что образующиеся при реакции спирты ( метилопый или этиловый) смешиваются с водой и легко летучи, так что их присутствие не усложняет выделения продуктов реакции. [1]
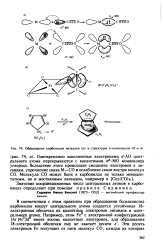 |
Образование карбонилов металлов ( а и структуры л-комплексов ( б и в. [2] |
Сиджвик Н вил Винсент ( 1873 - 1952) - английский профессор химии. [3]
Сиджвик, распространив теорию Льюиса на комплексные соединения, высказал мнение, что присоединение лигандов к комплексообразователю должно продолжаться до тех пор, пока последний не достигнет эффективного атомного номера, равного такому числу электронов, какое имеет ближайший инертный газ. [4]
Сиджвик [44] предположил, что оно содержит одноэлектронные связи. [5]
Сиджвик ( Sidgwick, 1950) укйзал на существование осмиевых комплексов с координационным числом девять или десять, хотя ни структурных, ни достоверных аналитических данных по этому вопросу не имеется. [6]
Сиджвик принял идеи Льюиса о двухэлектронной ковалент-ной связи между двумя атомами в молекуле и ввел понятие координационной связи для случая, когда оба электрона, образующие связь, поставляются одним атомом. Заметив, что все молекулы или ионы, которые могут присоединяться к иону металла, имеют по крайней мере одну неподеленную пару электронов, он предположил, что эта свободная электронная пара частично может быть отдана иону металла при образовании связи. Такую связь называют дативной или семиполярной и иногда изображают стрелкой ( М - L), которая указывает, что донорная группа ( L) поставляет на связь с акцептором ( М) оба электрона. [7]
Сиджвик [2] указал, что ковалентные связи могут образовываться двумя различными способами. Если каждый из двух соединяющихся атомов поставляет для образования связи по одному электрону, то он называет это нормальной ковалент-ностью; если же один из них ( донор) поставляет два электрона. [8]
Сиджвик развил представления Льюиса, предположив, что химическая связь может образовываться электронной парой, оба электрона которой принадлежат одному партнеру. Ясно, что при таком способе образования химической связи одна частица использует электронную пару другой, которая до этого момента была свободна. Частицу ( ион или молекулу), отдающую электронную пару, называют донором ( подателем), а частицу, присоединяющую электронную пару - акцептором ( приемником); связь, образованная таким путем, получила название донорно-акцеп-торной. [9]
Сиджвик пришел к выводу, что гидратация отрицательных ионов представляет собой исключение. Однако в некоторых случаях гидратация отрицательных ионон является твердо установленной и объясняет, например, существование гндратированных сульфатов с нечетным числом ( 1 5 7) молекул воды. [10]
Сиджвик [3] предполагает, что кислород сильнее как донор, чем протон как акцептор. Более важно то, что можно сравнить относительную кислотность воды с кислотностью других растворителей. [11]
Сиджвик принял идеи Льюиса о двухэлектронной ковалентной связи между двумя атомами в молекуле и ввел понятие координационной связи для случая, когда оба электрона, образующие связь, поставляются одним атомом. Заметив, что все молекулы или ионы, которые могут присоединяться к иону металла, имеют по крайней мере одну неподеленную пару электронов, он предположил, что эта свободная электронная пара частично может быть отдана иону металла при образовании связи. Такую связь называют дативной или семиполярной и иногда изображают стрелкой ( M - - L), которая указывает, что донорная группа ( L) поставляет на связь с акцептором ( М) оба электрона. [12]
Сиджвик [206] считает очевидным, что платина образует с СО химическое соединение, так как СО не вытесняется другими газами и его поглощению не препятствует предварительная обработка платины водородом. СО выделяется из платины при 250 С. [13]
 |
Равновесное распределение одинаковых. [14] |
Сиджвиком и Пауэллом в 1940 г.) расположение лигандов определяется взаимным отталкиванием донор-ных электронных пар, которые изображаются в виде точечных частиц, равноудаленных от центра катиона. [15]
Страницы: 1 2 3 4