Скорость
Cтраница 1
Скорость зависит от удельного сопротивления пыли, а оно, в свою очередь, зависит от электропроводности частиц пыли и присутствующей влаги. [1]
 |
Зависимость концентрации СА исходного вещества и концентрации са продукта реакции в одностадийном процессе А - Q от времени. [2] |
Скорость реакции1 может быть выражена также по изменению концентрации продукта реакции. [3]
Скорость такой реакции уже достаточно велика при - 80 С. С низкомолекулярными алканами реакция протекает легко. Хлор-ангидриды алкилфосфиновых кислот высокомолекулярных алканов термически устойчивы; их можно перегонять в вакууме. [4]
Скорость оказывается величиной переменной, меняющейся с течением времени в пределах от ит п - Ьа до чтах3 & со. [5]
Скорость v 2gR называется параболической или второй космической скоростью. Если считать Я о6378 км и gga 9 82 м / с2, то получим 2 11 2 км / с. Таким образом, при начальной скорости У0 11 2 км / с тело, брошенное с поверхности Земли под любым углом а к горизонтальной плоскости, будет двигаться по параболе или гиперболе ( при а90 - по прямой), неограниченно удаляясь от Земли. При скорости, меньшей второй космической, тело или упадет обратно на Землю, или станет искусственным спутником Земли. [6]
Скорость этого процесса пропорциональна квадрату концентрации активных центров ( квадратичный обрыв цепей) и общему давлению. Рекомбинация многоатомных радикалов обычно протекает по закону второго порядка, так как в результате перераспределения энергии по многим степеням свободы образующаяся при рекомбинации радикалов квазимолекула приобретает длительную стабильность и всегда имеет возможность передать избыточную энергию какой-либо сталкивающейся с нею молекуле или стенке. [7]
Скорость этого процесса пропорциональна квадрату концентрации активных центров ( квадратичный обрыв цепей) и общему давлению. Рекомбинация многоатомных радикалов обычно представляет собой бимолекулярный процесс, так как в результате перераспределения энергии взаимодействия радикалов по многим степеням свободы образующаяся при рекомбинации радикалов, квазимолекула приобретает длительную стабильность и всегда имеет возможность передать избыточную энергию какой-либо сталкивающейся с нею молекуле или стенке. Кроме того, повышенное содержание энергии в квазимолекуле иногда может привести к реакции днспропорционирования, в результате чего образуются две устойчивые молекулы. [8]
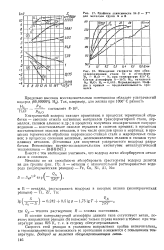 |
Графики зависимости In S - Т - для металлов групп А и В.| Изменение твердости при обезуглероживании стали 40 в атмосфере Н2 - Н2О - NJ при температуре 850 С. [9] |
Скорость этой реакции в указанном направлении крайне незначительна а термодинамическая возможность ее протекания понижается с повышением температуры. Водород не является обезуглероживающим газом. [10]
Скорости некоторых быстрых реакций могут быть также изучены с помощью метода абсорбции звука. [11]
Скорость некоторой реакции пропорциональна концентрации реагента и катализатора. Концентрация катализатора остается постоянной в течение опыта. Расчет с помощью интегрального метода показал, что реакция имеет первый порядок и константу скорости 5 8 X 10 - 6 сек-1. [12]
Скорость уменьшается введением объемных заместителей вблизи реакционного центра [11]; этот эффект добавляется к нормальным индуктивному и резонансному эффектам заместителей. [13]
Скорость, с которой полимерная цепь изменяет свою конфигурацию, определяет ее кинетическую гибкость. [14]
Скорость, с которой меняется свободная энергия при изменении концентрации отдельного вещества, называется химическим потенциалом системы, и Гиббсу удалось показать, что именно химический потенциал является движущей силой химических реакций. Химическая реакция идет самопроизвольно от точки с высоким химическим потенциалом к точке с низким химическим потенциалом, подобно тому как теплота самопроизвольно передается от точки с высокой температурой к точке с низкой температурой. [15]
Страницы: 1 2 3 4