Теплоемкость - водный раствор
Cтраница 1
Теплоемкость водного раствора принимают за единицу. [1]
Теплоемкости водных растворов неэлектролитов изучены менее систематично, чем энтальпии смешения, так что отсутствует возможность для широкого сопоставления величин Нв и Ср. Интерпретация довольно разрозненных данных о Ср для водных систем облегчается в какой-то мере, если предварительно рассмотреть поведение Ср и dCp / dT в более простых системах, для которых можно выделить определенные, превалирующие формы межмолекулярных взаимодействий. [2]
Теплоемкости водных растворов электролитов при 298 15 К и бесконечном разведении, как уже отмечалось, отрицательны и, например, в ряду щелочных галогенидов изменяются от 38 Дж / ( моль - К) у LiCl до - 134 3 Дж / ( моль - К) у Csl, у галогенидов щелочноземельных и других металлов величина АнСр еще более отрицательна. [3]
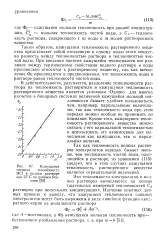 |
Кажущаяся мольная теплоемкость НС1 в водном растворе при 25 С по данным Россини. [4] |
Так как теплоемкость водных растворов электролитов нередко бывает меньше, чем теплоемкость чистой воды, находящейся в растворе, из уравнения ( 115) следует, что в этих случаях кажущаяся теплоемкость растворенного вещества является отрицательной величиной. [5]
Экспериментальные исследования теплоемкости водных растворов неэлектролитов немногочисленны и бессистемны. [6]
 |
Диаграмма кипения растворов серной кислоты при нормальном давлении. [7] |
С повышением температуры теплоемкость водных растворов кислоты возрастает. [8]
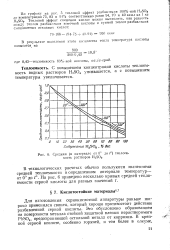 |
Средняя ( в интервале от 0 до t теплоемкость растворов HaSO. 1. [9] |
С повышением концентрации кислоты теплоемкость водных растворов H2SO4 уменьшается, а с повышением температуры увеличивается. [10]
С повышением концентрации кислоты теплоемкость водных растворов H2SO4 уменьшается, с повышением температуры - увеличивается. Безводная серная кислота имеет минимальную теплоемкость ( 0 338 кал / г град); теплоемкость олеума с повышением содержания SO3 ( своб. В технологических расчетах обычно пользуются значениями средней теплоемкости в определенном интервале температур. [11]
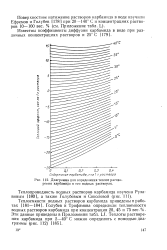 |
Диаграмма для определения теплот растворения карбамида в его водных растворах. [12] |
Голубев и Трофимова определили теплоемкости водных растворов карбамида при концентрации 20, 45 и 75 вес. Эти данные приведены в Приложении табл. LI. [13]
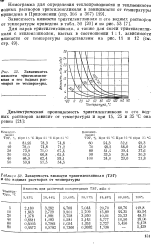 |
Зависимость вязкости триэтиленгликоля и его водных растворов от температуры.| Зависимость вязкости триэтиленгликоля ( ТЭГ и его водных растворов от температуры. [14] |
Номограмма для определения теплопроводности и теплоемкости водных растворов триэтиленгликоля в зависимости от температуры приведена в Приложении ( стр. [15]
Страницы: 1 2 3