Тетрамер
Cтраница 1
Тетрамер и тример реагируют аналогичным образом сами с собой, друг с другом, с мономером и димером. Поликонденсация идет, таким образом, ступенчато, причем молекулярный вес полимера непрерывно увеличивается. [1]
Тетрамер или высокополимер, будучи нагреты до 210, превращаются в нестабильный циклический тример, растворимый в органических растворителях, но легко переходящий в высокополимер. Тензиметрические определения в интервале 165 - 250 показывают, что тетрамер или высокополимер диссоциирует полностью с образованием тримера около 200, а при охлаждении легко превращается обратно в смесь высокополимеров. Измерения плотности пара и степени полимеризации представлены в табл. 1; данные серии 3 были получены со спиралью из плавленого кварца в качестве дифференциального манометра, чтобы избежать испарения ртути при высокой температуре. [2]
Тетрамер реагирует с хлором и образует Р ( СР3) СЦ. [3]
Тетрамер гидролизуется легче, чем тример; еще легче гидролизуются фосфонитрилбромиды и фосфонитрил-фториды. Реакция ускоряется в присутствии полярного растворителя, щелочи или третичного амина. [4]
Тетрамер является жидким веществом при комнатной температуре, однако имеет сравнительно высокую температуру кристаллизации. Для зонной плавки его не подходят методы, применимые как к высокоплавким, гак и к низкоплавким) соединениям. [5]
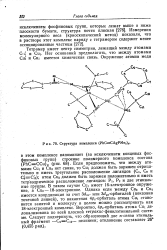 |
Структура комплекса. [6] |
Тетрамер имеет центр симметрии, лежащий между атомами C-i и GUI. Нет оснований предполагать, что между атомами Си и GUI имеется химическая связь. [7]
Тетрамер же образуется в незначительном количестве ( менее 4 %), в основном в виде примеси к тримеру. [8]
Тетрамер Со4 ( CO) ia является пирофорным твердым соединением, в инертном растворителе весьма стабилен. [9]
Тетрамер - кристаллическое вещество с температурой плавления 48 - 49, растворимое в органических растворителях. Пента-мер также представляет собой стабильное кристаллическое вещество с температурой плавления 120 - 121, растворимое в ацетоне и бензоле, но нерастворимое в воде и метиловом спирте. [10]
 |
Зависимость средних значений расстояний Мо-С ( СО от числа карбонильных групп, координированных атомом мо-либдена. [11] |
Тетрамер имеет так называемую кубановую структуру: четыре атома Мо и четыре группы ОН располагаются по вершинам куба, так что каждая группа ОН связывает три атома Мо, к каждому Мо примыкает три группы ОН. Координация Мо дополняется до октаэдрической двумя карбоксильными и одной нитрозогруппой, статистически занимающих три транс-позиции к группам ОН. Два других дикарбонильных соединения также имеют tfuc - строение. [12]
Тетрамер фосфонитрилхлорида гидролизуется легче, чем три-мер, с образованием тетрамерпой фосфонитрильной кислоты [ NP ( OH) 2 ] 4 2H20 [34, 36, 99], которая представляет собой весьма стабильные бесцветные кристаллы, слабо растворимые в воде. Образуя соли, кислота проявляет себя двух -, четырех - и восьмиосновной. [13]
Тетрамер аллена окисляется хамелеоном чрезвычайно легко. [14]
Тетрамер диметиларсиноборана начинает превращаться в тример при 180, тогда как тетрамер диметилфосфиноборана при этой температуре вполне устойчив. [15]
Страницы: 1 2 3 4