Углерод
Cтраница 1
Углерод, конечно, нельзя отнести к числу наиболее распространенных химических элементов. Но от всех остальных элементов он отличается исключительным разнообразием химических соединений. Число известных в настоящее время соединений углерода более чем вдвое превышает количество соединений всех остальных элементов, вместе взятых. [1]
Углерод в молекуле органического соединения, связанный лишь с одним атомом углерода ( например, крайние углеродные атомы в пропане), принято называть первичным; углерод, связанный с двумя атомами углерода ( например, средний углеродный атом в пропане), - вторичным; связанный с тремя углеродными атомами ( например, средний углеродный атом в изобутане) - третичным атомом; связанный с четырьмя углеродными атомами - четвертичным атомом углерода. [2]
Углерод в молекуле органического соединения, связанный лишь с одним атомом углерода ( например, крайние углеродные атомы в пропане), принято называть первичным; углерод, связанный с двумя атомами углерода ( например, средний углеродный атом в пропане), - вторичным; связанный с тремя углеродными атомами ( например, средний углеродный атом в изобутане), - третичным атомом; связанный с четырьмя углеродными атомами, - четвертичным атомом углерода. [3]
 |
Опудривающие и смазывающие материалы, применяемые в сухом виде или в виде специальных составов. [4] |
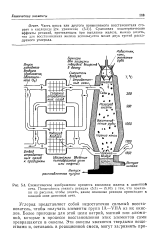
Углерод с примесями окислов кремния и железа. Кристаллизуется в мелкие гексагональные пластинки. Аморфный графит образуется в результате разложения органических соединений. Синтетический графит получают из нефтяного кокса разложением карборунда при 2000 С. [5]
Углерод представляет собой недостаточно сильный восстановитель, чтобы получать элементы групп IA-VIIA из их окислов. Более пригодны для этой цели натрий, магний или алюминий, которые в процессе восстановления этих элементов сами превращаются в окислы. [7]
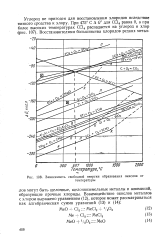 |
Зависимость свободной энергии образования окислов от. [8] |
Углерод не пригоден для восстановления хлоридов вследствие низкого сродства к хлору. [9]
Углерод ( алмаз) и кремний кристаллизуются в кубической системе, растворяются в расплавленных металлах и выделяются при охлаждении этих сплавов в элементарном виде. Оба элемента отличаются ярко выраженным восета ноз ительным характером. Они одинаково относятся к разбавленным соляной, серной и азотной кислотам, которые не окисляют кремний и углерод Tip и обыкновенной температуре. [10]
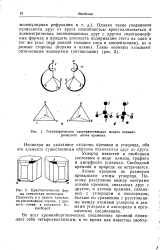 |
Тетраздрическая пространственная модель асимметрического атома кремния.| Кристаллические формы оптических антиподов. [11] |
Углерод известен в свободном состоянии в виде алмаза, графита и аморфного углерода. Свободный кремний в природе не встречается. [12]
Углерод образует метаугольную кислоту - Н2СОз, которая не устойчива и в момент своего образования легко разлагается на воду и двуокись углерода. Ортоугольная кислота Н4СО4 - не существует, хотя известны ее кальциевая соль - Са2СО4 и эфиры. [13]
Углерод некоторых кремнийоргани-ческих соединений в условиях мокрого окисления количественно окисляется до двуокиси углерода. [14]
 |
Работа развития трещины ( а и волокнистость излома ( б сталей с различным содержанием углерода при понижении температуры. [15] |
Страницы: 1 2 3 4 5