Енольная форма - ацетилацетон
Cтраница 1
Енольная форма ацетилацетона обладает умеренно кислыми свойствами ( К А - Ю-9; ср. Еноляты щелочных металлов могут быть проалкилированы алкил-галогенидами, достаточно реакционноспособными в 8к2 - реакциях; при этом, как правило, происходит С-алкилирование. Выходы лучше, чем при алкилировании по Халлеру - Бауэру, так как анионы с более слабыми основными свойствами реагируют по типу Е2 - отщепления ( см. стр. Ряд важных в синтетическом отношении реакций алкилирования других 1 3-дикарбонильных соединений будет рассмотрен в гл. [1]
Енольная форма ацетилацетона обладает умеренно кислыми свойствами ( / ( Ал 10 - 9; ср. Еноляты щелочных металлов могут быть проалкилированы алкилгалогенидами, достаточно реакцион-носпособными в 5к2 - реакциях; при этом, как правило, происходит С-алкилирование. Выходы лучше, чем при алкилировании по Хал-леру - Бауэру, так как анионы с более слабыми основными свойствами реагируют по типу Е2 - отщепления ( разд. Ряд важных в синтетическом отношении реакций алкилирования других 1 3-дикарбонильных соединений будет рассмотрен в гл. [2]
Енольная форма ацетилацетона обладает умеренно кислыми свойствами ( К А 10 - 9; ср. Еноляты щелочных металлов могут быть проалкилированы алкил-галогенидами, достаточно реакционноспособными в S - реакциях; при этом, как правило, происходит С-алкилирование. Выходы лучше, чем при алкилировании по Халлеру - Бауэру, так как анионы с более слабыми основными свойствами реагируют по типу Е2 - отщепления ( см. стр. Ряд важных в синтетическом отношении реакций алкилирования других 1 3-дикарбонильных соединений будет рассмотрен в гл. [3]
Енольная форма ацетилацетона обладает более выраженными кислотными свойствами, чем спирты, поэтому ацетилацетон легко образует с основаниями металлические производные - еноляты. [4]
От енольной формы ацетилацетона СН3 - СО - СНС ( ОН) - СНз производится интересный ряд металлических соединений - ацетил-ацетон атов железа, меди, алюминия, бериллия, хрома, кобальта и др. Они легко образуются при смешении с ацетилацетоном свежеосажденных гидроокисей этих металлов, взвешенных в воде. Обычно сначала осадки гидроокисей переходят в раствор, из которого затем выделяются труднорастворимые ацетилацетонаты. Многие из них способны возгоняться и даже перегоняться без разложения. Очень часто окраска этих веществ отличается от окраски обычных солей соответствующих металлов. [5]
 |
Энергии водородной связи в возбужденном состоянии. [6] |
В возбужденных молекулах типа метилсалицилата, метиловых эфиров о-окси-нафтойных кислот, енольных форм ацетилацетона и дибензоилме-тана, у которых энергия образования цикла с водородной связью может достигать 30 ккал / моль ( о-оксиазосоединения и о-оксиазоме-тиновые соединения), при п - я - переходе также должно наблюдаться значительное упрочнение квазиароматического цикла с водородной связью. В то же время соответствующие эфирные производные указанных соединений не обладают люминесцентными свойствами. [7]
Кето-енольная таутомерия зависит не только от молещ лярной структуры, но также и от природы растворителя: содержание енольной формы ацетилацетона в воде составляет 19 %, в хлороформе - 79 %, в бензоле - 85 % и в гексане - 92 % ( стр. [8]
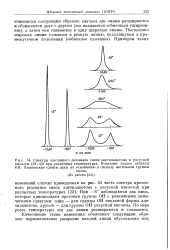
При - 8 наблюдаются два пика, которые приписывают протонам группы ОН с различными химическими сдвигами: один - для группы ОН енольной формы ацетилацетона, другой - для группы ОН уксусной кислоты. По мере роста температуры эти две линии расширяются и сливаются. [10]
Сильное изменение в спектре ацетилацетона происходит при добавлении уксусной кислоты. Возникает обмен между протонами ОН-группы енольной формы ацетилацетона и уксусной кислотой. В интервале температур 0 - 100 спектр ЯМР претерпевает последовательные изменения, связанные с переходом от медленного обмена к быстрому. Добавление диэтиламина также стимулирует быстрый протонный обмен и уширяет сигнал протона ОН-группы; кроме того, диэтиламин ускоряет переход между обеими формами ацетилацетона. Предполагается, что этот быстрый перенос протона обусловлен сильной водородной связью между молекулами ацетил-ацетона и диэтиламина. [11]
Дополнительными факторами, стабилизирующими енол форму ацетилацетона, являются сопряжение со второй л-св и образование внутримолекулярной водородной связи. Инте): отметить, что в енольной форме ацетилацетона реализу кроме того, динамический процесс иного типа - быстрая MI ция водорода между атомами кислорода. [12]
Ацетилацетон ( пентандион-2 4) реагирует с первичными аминами и образует имины. По существу при этом аналогично салициловому альдегиду реагирует енольная форма ацетилацетона. [13]
Страницы: 1