Антисимметричная функция
Cтраница 1
Симметричные и антисимметричные функции tys и о а описывают разные орбитальные движения электронов и поэтому им отвечают разные энергии. Какая энергия окажется меньше, зависит от конкретной задачи. В молекуле водорода минимальная энергия соответствует симметричной волновой функции, описывающей орбитальное движение. Именно поэтому электронный спин у Н2 равен нулю. [1]
Такая антисимметричная функция представляет собой детерминант. [2]
Набор антисимметричных функций % tm i где frtm - произведение собственных функций изолированных молекул, обладает и рядом других неприятных свойств. Функция Atynm шюр-тогональны друг другу. Помимо расчетных шудобств, гто означает, что функции А пт не могут быть собственными ни для какого эрмитова гамильтониана. К тому же набор Mw но япляотся полным, так как функции Фпш линейно пависимы. Доказательство последнего утверждения может быть проподело в болоо общем случае. [3]
Использование антисимметричной функции (111.63) показывает, что в этом случае молекула Н2 не образуется. Выясним физический смысл симметричной и антисимметричной волновых функций; в данном случае он несколько иной, чем в расчете молекулы Н2 по методу Гейтлера и Лондона, поскольку здесь рассматривается один электрон. [4]
Наоборот, антисимметричная функция отвечает такому состоянию, когда электроны имеют одинаково направленные, или параллельные, спины. [5]
Паули, антисимметричные функции правильно учитывают требования принципа Паули. Поэтому пригодными являются лишь антисимметричные волновые функции. [6]
 |
Экспериментальная ( / и теоретические ( 2 3 кривые энергии. молекулы водорода. Теоретические кривые рассчитаны с помощью симметричной ( 2 и антисимметричной ( 3 волновой функции. [7] |
Наоборот, антисимметричная функция отвечает такому состоянию, когда электроны имеют одинаково направленные, или параллельные спины. [8]
Наоборот, антисимметричная функция отвечает такому состоянию, когда электроны имеют одинаково направленные, или параллельные, спины. [9]
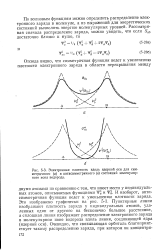 |
Электронная плотность вдоль ядерной оси для симметричного ( а и антисимметричного ( в состояний молекулярного иона водорода. [10] |
И наоборот, антисимметричная функция ведет к уменьшению плотности заряда. [11]
И наоборот, антисимметричная функция ведет к уменьшению плотности заряда. Очевидно, что связывающая орбиталь благоприятствует такому распределению заряда, при котором он концентрируется между ядрами, в то время как разрыхляющая орбиталь ведет к уменьшению плотности заряда в этой области и к концентрации его около индивидуальных атомных ядер. Так как ковалентная связь возникает при распределении электронного заряда в области связи, то очевидно, что только симметричная функция обусловливает образование устойчивой молекулы. [12]
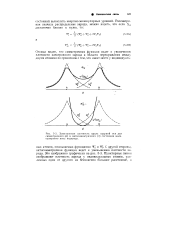 |
Электронная плотность вдоль ядерной оси для симметричного ( а и антисимметричного ( б состояния молекулярного иона водорода. [13] |
С другой стороны, антисимметричная функция ведет к уменьшению плотности заряда. [14]
Если из этих систем построить антисимметричные функции (3.16), то легко увидеть, что А и D исключаются принципом запрета, в то время как В к С оказываются не независимыми. Таким образом, остается только одна система, скажем, В, а так как для нее обе суммы значения для тг и та равны нулю, то терм будет типа 1SQ ( см. раздел 1 гл. [15]
Страницы: 1 2 3 4