Эндотермичность
Cтраница 1
Эндотермичность этой реакции составляет 17 ккал / моль, наблюдаемая энергия активации равна 37 ккал / моль. Поэтому высота энергетического барьера равна около 20 ккал / моль, что очень близко к значению 22 ккал / моль, определенному для бирадикала. [1]
Эндотермичность такой реакции составляет всего 20 ккал / моль. [2]
Эндотермичность этого процесса обусловливает необходимость получения ферромолибдена в электропечи. Применение углерода как восстановителя приводит к получению ферромолибдена с содержанием углерода более высоким, чем это допускается стандартом. [3]
Эндотермичность стадии ( 3) равна 35 ккал / моль, а энергия активации 39 ккал / моль. [4]
Эндотермичность стадии ( 1) составляет 32 ккал / моль, поэтому равновесие ( 1) быстро устанавливается. Затем следует экзотермическая реакция ( 3), имеющая энергию активации, вероятно, около 5 ккал / моль, после чего быстро образуется формальдегид. Энергия активации стадии ( 2), по-видимому, близка к 16 ккал / моль. Только в этой реакции образуется радикал, осуществляющий продолжение цепи. [5]
Эндотермичность атаки радикалом С ( СНз) з первичной связи С - Н равна 7 ккал / моль. [6]
Эндотермичность ацетилена обусловливает его взрывчатость при сжатии. [7]
Эндотермичность восстановления вызывает необходимость постоянного подвода тепла от источника, который, естественно, должен иметь более высокую температуру. [8]
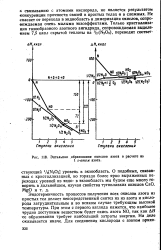 |
Энтальпии. образования окислов азота в расчете на 1 г-атом азота. [9] |
Эндотермичность процессов получения всех окислов азота из простых тел делает непосредственный синтез их из азота и кислорода затруднительным и во всяком случае требующим высокой температуры. При этом с первого, взгляда кажется, что наиболее трудно доступным веществом будет окись азота NO, так как АЯ - ее образования требует наибольшей затраты энергии. На деле оказывается иначе. [10]
Эндотермичность перехода закиси железа из шлака в металл определяет эндотермичный тепловой эффект реакции обезуглероживания металла под окислительным шлаком. [11]
Эндотермичность процесса конверсии метана можно частично восполнить энергией, выделяющейся при неполном его окислении. [12]
Вследствие эндотермичности этих реакций необходим подвод тепла, для чего обычно в печи сжигается генераторный или природный газ, компоненты которого ( Н2, СО, СН4) при неполном сжигании также восстанавливают барит. [13]
Ввиду эндотермичности все рассматриваемые реакции осуществляются в трубчатых контактных аппа-ратах. [14]
Вследствие эндотермичности процесса диссоциации константа равновесия возрастает с увеличением температуры, но даже при 3000 С и обычном давлении все еще не заметна диссоциация. Большая прочность связи N N в молекуле азота объясняет в принципе его химическую инертность. [15]
Страницы: 1 2 3 4