Энергия - сублимация
Cтраница 1
Энергия сублимации является той энергией, которую надо ввести в кристалл, чтобы перевести его в состояние свободных атомов или молекул. [1]
Энергия сублимации соединения влияет на прочность этого соединения в обратном направлении по сравнению с энергией атомизации простых веществ: чем больше ( по абсолютной величине) энергия сублимации, тем больше энергии выделится при переходе от газообразного вещества к твердому, следовательно, тем экзотермичнее будет твердое вещество. Так же, но в более слабой степени, на суммарную величину АЯобр влияет энергия испарения жидкого соединения. [2]
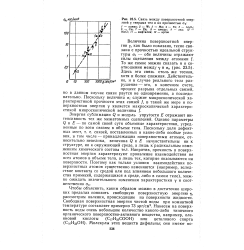 |
Связь между поверхностной энергией у твердых тел и их прочностью сгв. [3] |
Энергия сублимации Q и модуль упругости Е отражают интенсивность тех же межатомных сцеплений. Однако параметры Q и Е - по самой своей сути объемные характеристики, усредненные по всем связям в объеме тела. Q и Е нечувствительны ни к структуре, ни к окружающей среде, а лишь к радикальным изменениям химического состава тел. Напротив, прочность и поверхностная энергия характеризуют проявление взаимодействия не всех атомов в объеме тела, а лишь тех, которые оказываются на поверхности. Поэтому как только условия взаимодействия поверхностных атомов существенно изменяются ( например, вследствие контакта со средой или под влиянием небольшого количества примесей, содержащихся в среде, либо в самом теле), можно ожидать значительного изменения характеристики у и соответственно ств. [4]
Энергия сублимации кристаллов хлора равна 25 кДж / моль, а энергия диссоциации молекулы хлора равна 243 кДж / моль. [5]
Но энергия сублимации веществ с молекулярной решеткой X, равная в среднем 8 - 10 ккал / молъ, иногда достигает 1 - 2 ккал и редко - 12 - 15 ккал. [6]
Вхождение энергии сублимации в QAK и т - Д - а следовательно и в скорости реакции, является переходным звеном, связывающим мультиплетную теорию с теорией пересыщения С. Последняя полагает, что А тем больше, чем более удалена от равновесия реакция, служащая для приготовления катализатора. [7]
Зная энергию сублимации г и энтропию конденсата и выбрав по возможности такую температуру, когда одни степени свободы движения молекул пара полностью возбуждены, а другие, напротив, возбуждены столь мало, что заметно не проявляются ( и когда вследствие этого отпадает по - - правочный член эйнштейновских функций от характеристических температур пара, определение которых требует специального исследования), по формуле (6.19) можно вычислить химическую постоянную вещества по одной точке температурной кривой давления насыщенного пара. [8]
Так, энергии сублимации ионных соединений ( переход из твердого состояния в газообразное) обычно велики, например 50 - 60 ккал / моль для солей типа NaCl. Энергия сублимации кристаллических ковалентных соединений составляет всего примерно 10 ккал / моль. Ионные соединения имеют высокие точки плавления, в то время как несложные ковалентные соединения ( Н2, С12, СН4, SiH4, CF4, Sip4) при обычных условиях - газообразные вещества. Отличия ионных соединений от ковалентных в известной мере проявляются также при растворении их в воде. Водные растворы ионных соединений способны проводить электрический ток вследствие наличия в таких растворах свободных ( точнее - гидратиро-ванных) ионов. Ковалентные соединения зачастую вовсе нерастворимы в воде. В тех же случаях, когда ковалентные соединения растворяются в воде, их растворы не содержат ионов, а потому не проводят электрического тока. Следует, впрочем, применять этот критерий с осторожностью. [9]
По величине энергии сублимации межмолекулярные связи в типичных молекулярных решетках, также носящие дисперсионный характер, близки к связям в решетках кристаллизованных инертных газов с тем же числом электронов. Так, энергия сублимации азота ( число электронов в молекуле / 2 14) х 1 33 ккал / моль, энергия сублимации аргона ( Z i8) S r - 1 5 ккал / г-ат. [10]
По величине энергии сублимации межмолекулярные связи в типичных молекулярных решетках, также носящие дисперсионный характер, близки к связям в решетках кристаллизованных инертных газов с тем же числом электронов. [11]
В частности, энергия сублимации окиси кальция равна примерно - 150 ккал / моль. [12]
Ввный корню квадратному из энергии сублимации на единицу объема. [13]
Эвный корню квадратному из энергии сублимации на единицу объема. [14]
Легко сообразить, что энергия сублимации твердой [ ВеО ] будет сильно зависеть от того, в какой форме происходит испарение. [15]
Страницы: 1 2 3 4