Свободная энергия - образование - углеводород
Cтраница 1
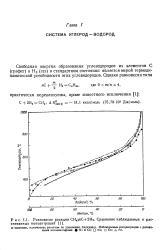 |
Равновесие реакции СН4 С 2Н2. Сравнение наблюдаемых и рассчитанных концентраций. [1] |
Свободная энергия образования углеводородов из элементов С ( графит) и Н2 ( газ) в стандартном состоянии является мерой термодинамической устойчивости этих углеводородов. [2]
Величины свободных энергий образования углеводородов из элементов при стандартной температуре 25 С 298 16 К необходимы для приближенных расчетов равновесий. [3]
Ниже приведены значения свободной энергии образования наиболее важных углеводородов, с которыми приходится встречаться при крекинг-процессах. Уравнения, представленные в табл. 18 [1], даны в упрощенной форме, которая, однако, вполне достаточна для наших целей. Имеются сведения о свободной энергии образования газообразных углеводородов из графита и газообразного водорода при температурах 700 - 1000 К. [4]
В главе б-й рассматриваются свободные энергии образования углеводородов и примеры приближенных расчетов равновесий реакций углеводородов. [5]
На рис. 1 приведены величины свободной энергии образования углеводородов. [6]
Вследствие этого ниже приводятся значения свободной энергии образования наиболее важных углеводородов и некоторых неорганических веществ, с которыми приходится иметь дело при процессах крекинга. Помещенные в табл. 22 данные [1] показывают изменения свободной энергии образования газообразных углеводородов ( если нет оговорки) из графита и газообразного водорода в температурном интервале 700 - 1000 К. [7]
Вследствие этого ниже приводятся значения свободной энергии образования наиболее важных углеводородов и некоторых неорганических веществ, с которыми приходится иметь дело при процессах крекинга. Помещенные в табл. 22 данные [1] показывают изменения свободной энергии образования газообразных углеводородов ( если нет оговорки) из графита и газообразного водорода в температурном интервале 700 - 1000 К. [8]
На рис. 9 изображена зависимость величин свободных энергий образования углеводородов от температуры; эти величины отнесены к 1 атому углерода. Зависимость от температуры исследована в пределах 700 - 1200 К. В связи с тем, что уравнения, приведенные ниже в табл. 18, будут использованы для вычислений равновесий при температурах более высоких, чем 1200 К, следует указать, что результаты, полученные экстраполированием за указанные пределы температур, нельзя считать вполне достоверными. Графический способ выражения зависимости свободной энергии образования, отнесенной к одному атому углерода, от температуры дает ясное представление об относительной стабильности индивидуальных углеводородов. [9]
На рис. 11 изображена зависимость величин изменений свободной энергии образования углеводородов от температуры в пределах 300 - 1200 К; эти величины отнесены к 1 атому углерода. [10]
На рис. 11 изображена зависимость величин изменений свободной энергии образования углеводородов от температуры в пределах 300 - 1200 К; эти величины отнесены к 1 атому углерода. [11]
Из графика видно, что с повышением температуры свободная энергия образования углеводородов различных рядов изменяется различным образом. Быстрее повышается свободная энергия метановых углеводородов и циклопарафинов. Свободная энергия ароматических углеводородов и этиленовых углеводородов увеличивается медленней. [12]
В пятой главе излагается вязкость паров углеводородов, в шестой - свободные энергии образования углеводородов и примеры приближенных расчетов реакций, в седьмой - материалы по Р, V, i-соотношениям и летучести углеводородов. [13]
Во второй главе выпуска рассматриваются тепловые и термодинамические свойства углеводородов ( автор - проф. Ряд разделов ( летучесть, теплосодержание, коэфициент Джоуля-Томсона, свободные энергии образования углеводородов и др.) не успел войти во вторую главу первого выпуска и будет помещен в последующих выпусках Справочника. [14]
 |
Тепло га образования некоторых углеводородов ( по. [15] |
Страницы: 1 2