Этар
Cтраница 1
Этар и Вила [806] рекомендуют при бензоилировании чувствительных аминов вводить в водный раствор кристаллический гидрат окиси бария и постепенно добавлять хлористый бензоил. [1]
Применение реакции Этара к этилбензолу и другим алкилбензолам не приводит к образованию исключительно продуктов бензильного окисления. [2]
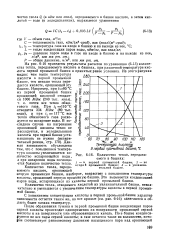 |
Количество тепла, передаваемого в башнях. [3] |
Это вызывается конденсацией этаров воды, испаряющихся из кислоты первой промывной башни. [4]
Заметим еще, что Этар недавно наблюдал образование камфорной кислоты ( свойства ее, впрочем, не описаны) при окислении камфоры красной кровяьой солью в щелочном растворе. [5]
Борнемаы [340] переработал реакцию Этара it общий метод; описываемые им толуиловые альдегиды в настоящее премя этим способом не получаются, но во многих случаях едва ли и и настоящее иремя можно получать более удобным способом и а мощенные ароматические альдегиды в не слишком больших количествах. Борпеман применил 15-и юцонт1ше растворы, Ворпер [341] для получения о - и л-бромбонлальдегидон исходил из 25 - 30-процентных раство-рон. При смошшщнии растворов во многих случаях наступает сильное разогревание, поэтому во избежание закипания сероуглерода смесь, в случае необходимости, охлаждают и, после добавления каждой новой порции хлористого хромила, ожидают, пока не иьтпадет диойное соединение шоколадного цвета. После некоторого стоя mm его отфильтровывают, из остатка па фильтре удаляют сероуглерод отсасыванием при умеренном нагревании и разлагают молекулярное соединение путем лнесенпя в холодную воду, при -, чем оно разлагается на альдегид, хлорный хром ( Gi Cl3) и хромовую кислоту. В зависимости от обстоятельств к л и тотчас же отгоняют альдегид с водяным паром, или обезвреживают хромовую кислоту пропусканием в смссг, сернистого газа. При больших загрузках окисление хлористым хромилом иногда может быть небезопасно, так как продукты присоединения могут неожиданно взорваться. [6]
Борнеман [340] переработал реакцию Этара в общий метод; описываемые им толуиловые альдегиды в настоящее время этим способом не получаются, но во многих случаях едва ли и в настоящее время можно получать более удобным способом замещенные ароматические альдегиды в не слишком больших количествах. [7]
Окисление углеводородов хромилхлоридом ( реактивом Этара), по-видимому, также протекает по радикальному механизму. Перванадил-ионы часто реагируют по радикальному механизму. Примером может служить гидроксилирование - углеродного атома в кетонах, которое быстро протекает под действием этого реактива. [8]
Хромовая кислота и хромилхлорид ( реагент Этара) также взаимодействует с парафиновыми углеводородами, причем по степени селективности их реакционная способность в основных чертах сходна с реакционной способностью атомов хлора. Восприимчивыми к такому действию являются а-положения боковой цепи ароматических соединений, третичные С - Н - группы парафинов и циклопарафннов и соседние с кислородом С - Н - группы простых эфиров; но стерических затруднений замечено не было и различия в реакционной способности между различными соединениями этих типов относительно невелики. Связи С-D атакуются медленнее, чем С - Н - связи. Кроме того, такие процессы окисления происходят медленнее при полном отсутствии кислорода, который поглощается реакционными смесями в слабой степени. Довольно любопытное окисление хромовой кислотой, катализируемое кислотами, протекает со скоростью, прямо пропорциональной общему содержанию хрома ( VI) в окисляемом растворе, и не является гетеролитическим окислением, как в случае спиртов, альдегидов и кетонов ( гл. [9]
В литературе имеются указания на то, что реакция Этара протекает с высокими выходами, достигающими 70 - 80 %, когда ее проводят в строго определенных условиях ( например, получение ж-толуилового альдегида из ж-ксилола), но могут получаться и значительно меньшие выходы. Метод находит лишь ограниченное применение. [10]
Изучение реакции окисления хлористым хромилом осложняется тем, что образующийся в качестве промежуточного соединения комплекс Этара не растворяется ни з одном из тех растворителей, с которыми он не реагирует. [11]
Прямое окисление ароматически или гетероциклически связанной метильной группы до альдегидной группы достигается хлористым хромилом по способу Этара, а также при применении определенных неорганических окислов, как перекись марганца или двуокись свинца. [12]
Высушивая хромовые квасцы при 110 С, Рекура [29] получил промежуточное тело Cr2 ( SO4) 3 - K SCvSHoO, растворявшееся подобно сернокислой соли Этара Сг2 ( 5С4) з 6Н2О весьма медленно в воде. [13]
В ней применяется двукратный мольный избыток хромилхлорида, растворителем служит дисульфид углерода, тетрахлорид углерода или хлороформ. Реакция Этара применима для синтеза ароматических альдегидов, содержащих нитрогруппы, галогены или алкильные заместители, хотя отличные от метальных ал-кильные группы могут окисляться предпочтительно. [14]
Сюда же следует отнести реактив Этара ( хлористый хромил) и триоксиметнлен ( Тауш) и формальдегид, переводящий бензол в формо-лит. Применение последней реакции более уместно в случае слабых концентраций бензола, позволяющих косвенное определение этого углеводорода по бензиновому остатку; выделение и определение этого остатка в массе формолита представляет непреодолимые затруднения, чуть дело касается аналитической точности работы. [15]
Страницы: 1 2