Квантовая ячейка
Cтраница 1
Квантовые ячейки изображены со сдвигом по вертикали, чтобы наглядно показать возрастание энергии в ряду li -, 2j -, 2р - состояний. Соответствующие схемы в третьей - асти книги даны без сдвига ячеек. [1]
Квантовые ячейки изображены со сдвигом по вертикали, чтобы наглядно показать возрастание энергии в ряду 15, 2s, 2р - состояний. Соответствующие схемы в третьей части книги даны без сдвига ячеек. [2]
Квантовые ячейки изображены со сдвигом по вертикали, чтобы наглядно показать возрастание энергии в ряду Is, 2s, 2р - состояний. Соответствующие схемы в третьей части книги даны без сдвига ячеек. [3]
Квантовые ячейки изображены со сдвигом по вертикали, чтобы наглядно показать возрастание энергии в ряду Is -, 2s -, 2р - состояний. Соответствующие схемы в третьей: асти книги даны без сдвига ячеек. [4]
Число квантовых ячеек в подгруппе определяется магнитным квантовым числом и растет как ряд нечетных чисел. Пирамидальная схема ( рис. 1.2) может быть продолжена до бесконечности м оо. [5]
В квантовой ячейке Не, изображенной справа, направление спинов указано вертикальными стрелками. [6]
В квантовых ячейках с одинаковой энергией заселение электронами происходит так, чтобы атом имел наибольшее число неспаренных электронов. У каждого последующего элемента Периодической системы на один электрон больше по сравнению с предыдущим. Наиболее прост первый период Системы, состоящий лишь из двух элементов. У водорода единственный электрон заселяет наинизшую энергетическую орбиталь Is, а у гелия на этой же орбитали два электрона с антипараллельными спинами. Таким образом, атом гелия полностью формирует наиболее близкий к ядру Д - слой. [7]
При заполнении квантовых ячеек электронами необходимо руководствоваться правилом Гунда: в данном подуровне электроны стремятся занять свободные квантовые ячейки сначала по одному с параллельными спинами и затем только по второму с противоположным направлением спина. По принципу Паули в каждой ячейке может быть только два электрона с противоположными спинами. При таком способе заполнения квантовых ячеек одного подуровня данным числом электронов суммарный спин имеет наибольшее значение, что требует правило Гунда. [8]
При заполнении квантовых ячеек необходимо знать правило Гунда: устойчивому состоянию атома соответствует такое распределение электронов в пределах энергетического подуровня ( р, d, f), при котором абсолютное значение суммарного спина атома максимально. Так, если два электрона займут одну орбиталь п I I, то их суммарный спин будет равен нулю. Заполнение электронами двух орбиталей т IТI I даст суммарный спин, равный единице. [9]
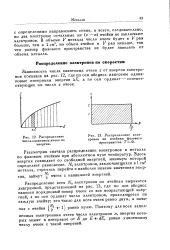 |
Распределение электронов по ячейкам фазового пространства Т 0. [10] |
Зависимость числа квантовых ячеек z от энергии электронов показана на рис. 12, где по оси абсцисс нанесены одинаковые интервалы энергии Е, а по оси ординат - соответствующее им число z ячеек. [11]
Другими словами, квантовые ячейки подуровня заполняются сначала по одному электрону, а затем по второму с противоположно направленным спином. Так, у атома азота ( рис. 9) в трех / - ячейках разместятся три электрона по одному в каждой, в атоме три неспаренных электрона. Если же предположить иное размещение электронов, например, в одной ячейке 2, в другой 1 и третья пустая, то 2s 1 / 2 - 1 / 2 1 / 2 1 / 2, что противоречит правилу Гунда. [12]
Распределение электронов по квантовым ячейкам ( см. рис. 1.34) показывает, что в атоме фтора имеется только один неспаренный электрон, поэтому фтор одновалентен. [13]
 |
Электронная структура атома кислорода в виде квантовых ячеек. [14] |
Однако на рис. 19 квантовые ячейки для данного слоя ( квантовое число п постоянно) изображены на одной горизонтали, хотя в действительности существуют небольшие различия в энергиях разных орбиталей. [15]
Страницы: 1 2 3 4