Квантовая ячейка
Cтраница 2
Число и взаимное расположение квантовых ячеек на последней схеме показывает, что: 1) электроны в атоме лития расположены на двух энергетических уровнях, причем первый из них состоит из одного подуровня ( Is) и целиком заполнен; 2) второй - внеш ний - энергетический уровень соответствует более высокой энергии и состоит из двух подуровней ( 2s и 2р); 3) 2-подуровень включает одну орбиталь, на которой в атоме лития находится один электрон; 4) 2р - подуровень включает три энергетически равноценные орбитали, которым соответствует более высокая энергия, чем энергия, отвечающая 25-орбитали; в невозбужденном атоме лития 2р - орбитали остаются незанятыми. [16]
Число и взаимное расположение квантовых ячеек на последней схеме показывает, что: 1) электроны в атоме лития расположены на двух энергетических уровнях, причем первый из них состоит из одного подуровня ( Is) и целиком заполнен; 2) второй - внешний - энергетический уровень соответствует более высокой энергии и состоит из двух подуровней ( 2s и 2р); 3) 25-подуровень включает одну орбиталь, на которой в атоме лития находится один электрон; 4) 2р - подуровень включает три энергетически равноценные орбитали, которым соответствует более высокая энергия, чем энергия, отвечающая 25-орбитали; в невозбужденном атоме лития 2р - орбитали остаются незанятыми. [17]
Число и взаимное расположение квантовых ячеек на последней схеме показывает, что: 1) электроны в атоме лития расположены на двух энергетических уровнях, причем первый из них состоит из одного подуровня ( Is) и целиком заполнен; 2) второй - внешний - энергетический уровень соответствует более высокой энергии и состоит из двух подуровней ( 2s и 2р); 3) 25-подуровень включает одну орбиталь, на которой в атоме лития находится один электрон; 4) 2р - подуровень включает три энергетически равноценные орбитали, которым соответствует более высокая энергия, чем энергия, отвечающая 25-орбитали; в невозбужденном атоме лития 2р - орбитали остаются незанятыми. [18]
Число и взаимное расположение квантовых ячеек на последней схеме показывает, что: 1) электроны в атоме лития расположены на двух энергетических уровнях, причем первый из них состоит из одного подуровня ( Is) и целиком заполнен; 2) второй - внешний - энергетический уровень соответствует более высокой энергии и состоит из двух подуровней ( 2s и 2р); 3) 25-подуровень в клю-чает одну орбиталь, на которой в атоме лития находится один электрон; 4) 2р - подуровень включает три энергетически равноценг ные орбитали, которым соответствует более высокая энергия, чем энергия, отвечающая 25-орбитали; в невозбужденном атоме лития 2р - орбитали остаются незанятыми. [19]
Число и взаимное расположение квантовых ячеек на последней схеме показывает, что: 1) электроны в атоме лития расположены на двух энергетических уровнях, причем первый из них состоит из одного подуровня ( Is) и целиком заполнен; 2) второй - внешний - энергетический уровень соответствует более высокой энергии и состоит из двух подуровней ( 2s и 2р); 3) 25-подуровень включает одну орбиталь, на которой в атоме лития находится один электрон; 4) 2р - подуровень включает три энергетически равноценные орбитали, которым соответствует более высокая энергия, чем энергия, отвечающая 25-орбитали; в невозбужденном атоме лития 2р - орбитали остаются незанятыми. [20]
Число и взаимное расположение квантовых ячеек на последней схеме показывает, что: 1) электроны в атоме лития расположены на двух энергетических уровнях, причем первый из них состоит из одного подуровня ( Is) и целиком заполнен; 2) второй - внешний - энергетический уровень соответствует более высокой энергии и состоит из двух подуровней ( 2s и 2р); 3) 25-подуровень включает одну орбиталь, на которой в атоме лития находится один электрон; 4) 2 / 7-подуровень включает три энергетически равноценные орбитали, которым соответствует более высокая энергия, чем энергия, отвечающая 25-орбитали; в невозбужденном атоме лития 2р - орбитали остаются незанятыми. [21]
Число и взаимное расположение квантовых ячеек на последней схеме показывает, что: 1) электроны в атоме лития расположены на двух энергетических уровнях, причем первый из них состоит из одного подуровня ( Is) и целиком заполнен; 2) второй - внешний - энергетический уровень соответствует более высокой энергии и состоит из двух подуровней ( 2s и 2р); 3) 25-подуровень включает одну орбиталь, на которой в атоме лития находится один электрон; 4) 2р - подуровень включает три энергетически равноценные орбитали, которым соответствует более высокая энергия, чем энергия, отвечающая 25-орбитали; в невозбужденном атоме лития 2р - орбитали остаются незанятыми. [22]
Изобразите распределение электронов по квантовым ячейкам в атомах брома, серы и азота. [23]
Схема распределения электронов по квантовым ячейкам помогает выявлять число неспаренных электронов в атоме и валентность эле - мента. [24]
Схема распределения электронов по квантовым ячейкам помогает выявлять число неспаренных электронов в атоме и валентность элемента. Она дает возможность показать и строение отдельных подуровней. [25]
Схема распределения электронов по квантовым ячейкам атома азота дана в § 2.7. Из нее легко сделать вывод, что поскольку азот имеет три неспаренных электрона, его валентность равна трем. [26]
Схема распределения электронов по квантовым ячейкам атома азота дана в § 2.7. Из нее легко сделать вывод, что поскольку азот имеет три неспаренных электрона, он может образовывать три химические связи и его валентность равна трем. [27]
Здесь электроны изображены в виде квантовых ячеек. В каждой квантовой ячейке возможно размещение только двух электронов с противоположными спинами. [28]
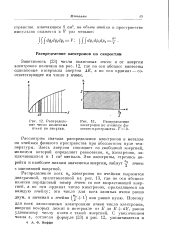 |
Распределение числа КЛНВТОРЫХ ячеек по энергии.| Распределение электронов по ячейкам фазового пространства. Т 0. [29] |
Зависимость ( 23) числа квантовых ячеек z от энергии электронов показана на рис. 12, где по оси абсцисс нанесены одинаковые интервалы энергии & Е, а по оси ординат - соответствующее им число z ячеек. [30]
Страницы: 1 2 3 4