Выход - перекись - водород
Cтраница 1
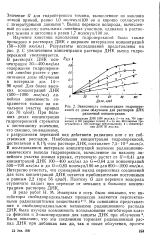 |
Зависимость концентрации гидроперекисей от дозы облучения для растворов ДНК различной концентрации. [1] |
Выход перекиси водорода, вычисленный по наклону начальных линейных участков, одинаков в растворах тимина и цитозина и равен 1 7 молекул / 100 эв. [2]
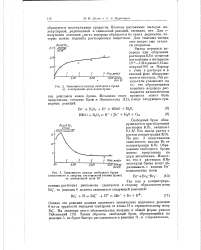 |
Зависимость выхода свободного брома от электронной доли ионов брома.| Зависимость выхода свободного брома ( отнесенного к энергии, поглощенной ионами брома от электронной доли Вг -. [3] |
Выход перекиси водорода при облучении растворов КВг остается постоянным в интервале 1 ( Г5 - 1Ми равенО 12мо - лекулы / 100 эв. [4]
Выход перекиси водорода резко уменьшается по мере увеличения плотности тока. С повышением плотности катодного тока, очевидно, происходит перерождение поверхности электрода, число адсорбционных центров, на которых адсорбированы молекулы кислорода, уменьшается, а число центров, на которых адсорбированы кислородные атомы, увеличивается. Восстановление же кислородных атомов дает не перекись водорода, а воду. [5]
Выход перекиси водорода под действием рентгеновских, у - и р-лучей оказывается значительным только в том случае, если вода содержит растворенный кислород. При отсутствии кислорода указанные реакции протекают с очень небольшим выходом. При радиолизе под действием а-частиц выход перекиси водорода в воде, насыщенной кислородом и полностью свободный от него, одинаков. [6]
Выход перекиси водорода достигает 90 % от теоретического, считая на израсходованный водород. [7]
Выход перекиси водорода зачастую значительно превышает вычисленный из закона Фарадея, но падение потенциала в этом случае на один или несколько порядков превышает падение, встречающееся в процессах электролиза. Выход зависит от природы электролита, рН раствора, природы газа, в котором происходит электрический разряд, давления газа, а также и от направления электрического тока. Клемелц [48] сообщил, что из серной кислоты в присутствии кислорода могут быть получены перекись водорода, пероксосерная и пероксодисерная кислоты с выходом, примерно в три раза превышающим выход по закону Фарадея; при добавлении станната натрия, играющего роль ингибитора разложения перекиси водорода, выход был примерно в 12 раз больше, чем по закону Фарадея. [8]
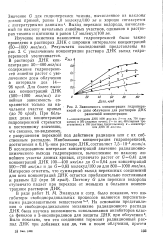 |
Зависимость концентрации гидроперекисей от дозы облучения для растворов ДНК различной концентрации. [9] |
Выход перекиси водорода, вычисленный по наклону начальных линейных участков, одинаков в растворах тимина и цитозина и равен 1 7 молекул / 100 эв. [10]
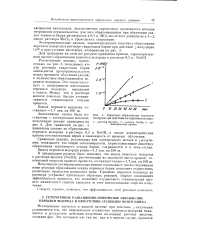 |
Кинетика образования перекиси водорода при действии электронного потока. [11] |
Выход перекиси водорода составляет - 1 7 экв. [12]
Выход перекиси водорода в водных растворах NaOH в присутствии кислорода незначителен и составляет - 1 7 экв. В пределах доз - 1020 эв / мл наблюдается, для применявшейся мощности дозы, линейный ход кинетических кривых. [13]
Выход перекиси водорода достигает 90 % от теоретического, считая на израсходованный водород. [14]
Выход перекиси водорода можно повысить, увеличив концентрацию кислорода в растворе. Это достигается осуществлением более тесного контакта амальгамы и раствора за счет интенсивного перемешивания и проведения реакции на специальном носителе, повышением концентрации кислорода за счет повышения давления до 25 - 30 ат и понижения температуры до 0 С. Выход перекиси водорода повышается добавлением стабилизирующих ее веществ - фторидов, боратов, цианидов, азотистых соединений, фенола. [15]
Страницы: 1 2 3 4