Акцептор - электрон
Cтраница 1
Акцептор электронов для ФСП и мягкий окисл. Восстановление может сопровождаться уменьш. Восстанавливается в нескольких местах вдоль электронотранспортной цепи. [1]
Акцептор электронов 102 Алании 641 Алкадпены 477 ел Ал ка нолы 527 с.л. Алкансульфокислоты 455 Ал капы 449 ел. [2]
Акцептор электронов покрыт слоем белковых молекул, действующих как некоторый экран, делающий его малочувствительным к внешним воздействиям. Кроме того, эти молекулы осуществляют связь акцептора Хт с комплексом молекул пластохинона. [3]
Акцепторы электронов ( кислоты) Мулликен разделяет на я-акцепторы, например полинитроароматические соединения, которые обладают ярко выраженной склонностью присоединять я-основания ( и которые мы почти не будем рассматривать), на ионные ( t) кислоты, например протон, и на кислоты с вакантными орбиталями ( и), например электрононенасыщенные галогениды металлов типа катализаторов реакции Фриделя - Крафтса, которые имеют особую склонность присоединяться к - основаниям. Галогены, так же как и галогеноводороды, могут присоединяться как к я -, так и к n - основаниям. Движущей силой взаимодействия в обоих случаях является высокая электроотрицательность атома галогена. Для того чтобы атом галогена мог принять отрицательный заряд передаваемого ему электрона, он должен ослабить свою уже имеющуюся ковалентную связь с другим атомом галогена или с водородом, что приводит, когда это возможно, к диссоциации. Хотя галогеноводороды и являются довольно слабыми кислотами Льюиса, в тех случаях, когда неблагоприятное окружение препятствует диссоциации, они могут стать очень сильными кислотами Брен-стеда, если имеются подходящие условия сольватации и диэлектрическая проницаемость растворителя достаточно высока. [4]
Акцепторы электронов ( тип I) притягивают it - электроны доноров. Поглощение в спектрах, вызванное переходом электронов ( перенос заряда), подтверждает донорно-акцепторное взаимодействие. [5]
Акцептором электронов здесь выступает НАДФ - специфический кофермент глюкозо-6 - фосфат - дегидрогеназы. Такое соединение нестабильное и спонтанное, хотя и ферментативное, гидролизуется до свободной кислоты. Этот гидролиз катализирует специфичный фермент лактоназа. [6]
Акцептором электронов служит молекулярный кислород. [7]
Акцепторами электронов могут быть также НАДФ, тиамин-липоевая кислота и некоторые другие вещества. Ва всех этих случаях хлорофилл остается в окисленном состоянии, тогда как второй компонент комплекса восстанавливается. [8]
Типичными акцепторами электронов для реакций, где промежуточным звеном служат бактерии, являются кислород, нитраты, сульфат и двуокись углерода. При использовании кислорода в качестве акцептора электронов выделяется максимальное количество энергии, при использовании двуокиси углерода - минимальное. Кроме того, при использовании в качестве акцепторов энергии нитритов, образованных в процессе нитрификации, энергии выделяется больше, чем при использовании кислорода. [9]
Хорошими акцепторами электронов для PS П являются п-фенилендиамины. [10]
Будучи хорошим акцептором электронов, малеиновый ангидрид легко образует молекулярные комплексы с рядом ненасыщенных соединений. [11]
Физиологическим конечным акцептором электрона в реакциях, катализируемых ксантино-ксидазой, является молекулярный кислород, однако в этом качестве могут также выступать цитохром с, ферритин, метиленовый синий. Субстратная специфичность ксантиноксидазы также не слишком велика. В качестве субстратов ксантиноксидаза может использовать более сотни соединений. К ним относятся прежде всего пурины и родственные им гетероциклические соединения, а также альдегиды. Константы связывания альдегидных субстратов примерно в 100 раз превышают константы связывания пуринов. [12]
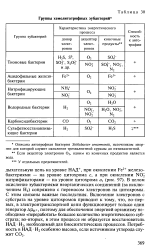 |
Группы хемолитотрофных эубактерий. [13] |
Если акцептор электронов 02, одним из конечных продуктов является вода. [14]
Атом акцептора электронов имеет НВО с высокой энергией, малый положительный заряд, большой размер и легко возбудимые внешние электроны. К мягким кислотам относятся легко поляризующиеся катионы металлов ( Си, Hg2, Pd2, Pt2, T1, Cd2) и органические соединения, способные принимать пару электронов на разрыхляющую я-орбиталь, например тетрацианоэтилен. [15]
Страницы: 1 2 3 4