Горение - метан
Cтраница 4
Определим в качестве примера теоретическую температуру горения метана, т.е. природного газа. [46]
Требуется определить значение константы равновесия реакции горения метана в кислороде СН4 2О2 СО2 2Н2О при температуре 950 С. [47]
Приведенная схема относится к начальной стадии горения метана. Здесь активной частицей является формальдегид. Окончательное окисление до СО2 и Н2О осуществляется на следующей стадии. [48]
Ниже приведен один из предположительных механизмов горения метана. [49]
Это обусловлено тем, что объем продуктов горения метана, примерно в 3 5 раза больше, чем объем продуктов горения водорода. Следовательно, для нагрева их до той же самой температуры в первом случае потребуется тепла в 3 5 раза больше, чем во втором. [50]
Лавровым и Петренко [10, 11] предлагается предположительный механизм горения метана при повышенных температурах, основанный на следующих положениях. [51]
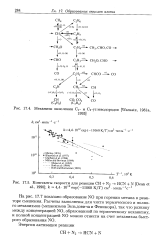 |
Механизм окисления Ci - и Сз-углеводородов [ Warnatz, 1981a.| Константы скорости для реакции СН N2 - HCN N [ Dean et al., 1990 ]. k 4 4 1012 exp ( - 11060 К / Г см3. [52] |
На рис. 17.7 показано образование N0 при горении метана в реакторе смешения. [53]
Подсчитанная аналогичным образом по упрощенной методике теоретическая температура горения метана равна 1930 С или - 2200 К. [54]
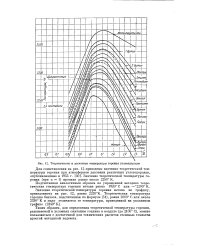 |
Теоретические и расчетные температуры горения углеводородов. [55] |
Подсчитанная аналогичным образом по упрощенной методике теоретическая температура горения метана равна 1930 С или - 2200 К. [56]
Страницы: 1 2 3 4