Два - атом - хлор
Cтраница 1
Два атома хлора объединяются в молекулу и выделяются на аноде в виде пузырьков газообразного хлора. Положительный ион при соприкосновении с катодом присоединяет к себе недостающие электроны и становится нейтральным атомом: Znr - r - - 2e - Zn. Металлический цинк осаждается на катоде. [1]
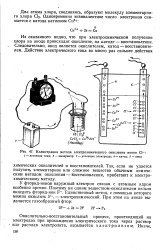 |
Иллюстрация метода электрохимического окисления ионов С1. У - источник тока. 2 - амперметр. 3 - угольные электроды. 4 - катод. 5 - анод. [2] |
Два атома хлора, соединяясь, образуют молекулу элементарного хлора СЬ. [3]
Два атома хлора вызывают больший сдвиг в слабое поле. [4]
 |
Схема образования длины связей. 7 - 206 пм. 2 - 206 пм. 3 и 4 - по 221 пм. [5] |
Два атома хлора в молекуле Ch образуют ковалентную связь по обменному механизму, объединяя свои неспаренные Зр-элект-роны. [6]
Дихлорпроизводные, содержащие два атома хлора при одном атоме углерода ( геминальные), взаимодействуя с водным раствором щелочи или с водой, образуют альдегиды или кетоны. Взаимодействуют с фторидами с образованием фторпроиз-водных углеводородов. При контакте с открытым пламенем и нагретыми поверхностями вследствие термического разложения выделяют фосген. [7]
 |
Образование молекулы хлора. [8] |
Когда два атома хлора приближаются друг к другу, одиночные электроны первого и второго атомов образуют общую пару электронов. [9]
Поэтому два атома хлора отталкиваются и предпочитают образовывать связи с кислородом. [10]
При реакциях два атома хлора замещаются сряшштсльш легко. Замещение третьего атома хлора притекает в более жестких условиях. [11]
Когда сближаются два атома хлора, у них появляется возможность образовать прочную ковалентную связь за счет обобществления двух электронов с полузаполненных валентных орбиталей. Когда же сближаются две молекулы хлора, они оказываются примерно в таком же затруднительном положении, как сближающиеся атомы аргона. Благодаря обобществлению электронов в молекуле каждый из атомов уже заполнил все свои валентные орбитали. Он может взаимодействовать и обобществлять электроны с другой молекулой хлора, только используя внешние орбитали, расположенные за пределами валентных орбиталей. [12]
Представим себе два атома хлора. При ковалентном связывании каждый из двух атомов хлора приносит в обобществленную пару электронов по одному электрону: образуется молекула хлора - СЬ. Поделенную пару электронов принято обозначать как одинарную связь: С-С. [13]
Следовательно, два атома хлора в основании квадрата оказываются более или менее блокированными, и только один атом остается до некоторой степени открытым. [15]
Страницы: 1 2 3 4
