Алкилфторид
Cтраница 1
Алкилфториды - реакционноспособные соединения: атом фтора в них может замещаться другими атомами и группами. Но при наличии в молекуле у одного атома углерода хотя бы двух атомов фтора подвижность последних резко снижается. Поэтому перфторуглероды очень устойчивы, не разлагаются даже при 500 С. [1]
Алкилфториды можно приготовить взаимодействием спирта и фтористого водорода, но эта реакция обратима. Максимальный выход ( 43 %) был получен при взаимодействии эквимолекулярных количеств кислоты и спирта. [2]
Колебательно возбужденные алкилфториды были получены при рекомбинации радикалов, образующихся при фотолизе фторированных альдегидов и кетонов. [3]
Комплексы алкилфторидов и кислот Льюиса нередко являются стабильными и могут быть выделены. [4]
Получение алкилфторидов из спиртов используется значительно реже, чем предыдущие реакции. Обычно фторирование осуществляют фтористоводородной кислотой в пиридине. Кроме того, применяют такие фторпроизводные серы, как Sp4 [ Ang. [5]
По-видимому, алкилфториды с магнием вообще не реагируют, потому что энергия связи С-F очень велика. [6]
Физиологическое действие алкилфторидов в дальнейшем объясняется их тенденцией отщеплять фтористый водород. [7]
Итак, единственными устойчивыми алкилфторидами являются низшие фторпроизводные, при разложении которых при обычных температурах образовался бы газообразный алкен или метиленовый радикал. Но, с другой стороны, ароматические фториды являются относительно устойчивыми и малореакционноспособными соединениями. [8]
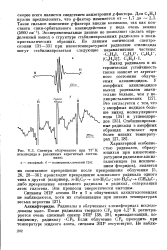 |
Спектры облученного при 77 К этилиодида в различных агрегатных состояниях. [9] |
Радикалы в облученных алкилфторидах исследо-дованы мало. Если облучение CF4 проводить при температуре жидкого азота, сигналы ЭПР отсутствуют. [10]
Вместо поляризованного комплекса алкилфторида с фтористым бором в реакции алкилирования может участвовать карбониевый ион, образующийся при взаимодействии BF3 с соответствующим алкилфторидом. Следовательно, механизм алкилирования зависит от строения алкилгалогенида. Соображения, высказанные относительно механизма реакций алкилирования, применимы к другим реакциям типа электро-фильного замещения, в том числе к реакциям кислотного водородного обмена в ароматических соединениях. [11]
Низкая реакционная способность алкилфторидов отличает их от других органических галогенидов, что, по-видимому, связано с большой прочностью связи С - F. Низкая реакционная способность ал-кшшитратов показывает, что слабый нуклеофил не обязательно всегда является легко замещаемой уходящей группой. [12]
При алкилировании изопарафинов алкилфторидами в присутствии, фтористого водорода образуются продукты, аналогичные продуктам, получаемым при алкилировании олефинами, за исключением того, что получается больше продуктов, образующихся по реакции переноса водорода. [13]
Превращение алкилталогенидов RGH2X в алкилфториды с помощью KF: исходит в этиленгликоле или, лучше, в диэтиленгликоле без доступа влаги при интен СИЕНОМ перемешивании. Необходимо вводить не менее 2 моль безводного KF на 1 м о. [14]
На практике целесообразно разлагать алкилфториды в системе катализатор - очиститель не полностью. Для разложения оставшейся части используют боксит с низким содержанием силикагеля. Боксит действительно реагирует с выделяющейся HF, и его следует заменять по мере потери им реакционной способности. Реакция идет при температуре 100 - 11О С. [15]
Страницы: 1 2 3 4