Зависимость - количество - адсорбированное вещество
Cтраница 1
Зависимость количества адсорбированного вещества от равновесной концентрации в растворе необходимо знать при расчете кинетики и динамики адсорбции, а также при расчете удельного расхода адсорбента при любом способе технологического оформления адсорбционного процесса. [1]
Зависимость количества адсорбированного вещества ( ПАВ) от равновесного давления ( или концентрации) при постоянной темпе - ратуре, т.е. графики а f ( p) или о - f ( c) при Т const, называются изотермами адсорбции. [2]
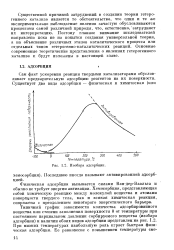 |
Изобара адсорбции. [3] |
Типичный график зависимости количества адсорбированного вещества или степени заполнения поверхности 6 от температуры при постоянном парциальном давлении сорбируемого вещества ( изобара адсорбции) и наличии обоих видов адсорбции представлен на рис. 1.2. При низких температурах наибольшую роль играет быстрая физическая адсорбция. [4]
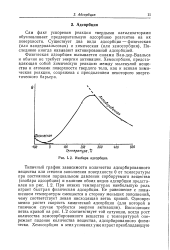 |
Изобара адсорбции. [5] |
Типичный график зависимости количества адсорбированного вещества или степени заполнения поверхности 0 от температуры при постоянном парциальном давлении сорбируемого вещества ( изобара адсорбции) и наличии обоих видов адсорбции представлен на рис. 1.2. При низких температурах наибольшую роль играет быстрая физическая адсорбция. Ее равновесие с повьь шением температуры смещается в сторону меньших заполнений, чему соответствует левая нисходящая ветвь кривой. Восходящая ветвь кривой на рис. 1.2 соответствует той ситуации, когда рост количества хемосорбированного вещества с температурой опережает падение количества вещества, адсорбированного физически. [6]
Однако известны случаи, когда зависимость количества адсорбированного вещества от концентрации раствора существенно отличается от изображенной на рис. 5.1. Это может быть вызвано образованием на поверхности адсорбента не моно -, а полимолекулярного слоя, что не предусматривается теорией Лэнг-мюра, а также тем, что поверхность реальных твердых тел неоднородна, и некоторыми другими причинами. [7]
В теоретических выводах изотерм адсорбции, выражающих зависимость количества адсорбированного вещества от равновесного давления присутствующего газа или от равновесной концентрации одновременно присутствующего растворенного вещества, в большинстве случаев предполагается, что теплота адсорбции имеет одно и то же значение для всей поверхности адсорбента. Подобная точка зрения, как было показано в разделе V, 12, едва ли может считаться справедливой по отношению к реальным адсорбентам. [8]
Были выдвинуты теории для объяснения особенностей адсорбционных процессов и выведены уравнения, характеризующие зависимость количества адсорбированного вещества от давления, температуры и других условий. [9]
Методы адсорбции из растворов аналогично методам адсорбции из газовой фазы основаны на экспериментальном построении изотерм - зависимостей количества адсорбированного вещества от его концентрации в растворе и нахождении величины адсорбции, соответствующей емкости монослоя. [10]
Методы адсорбции из растворов аналогично методам адсорбции из газовой фазы основаны на экспериментальном построении изотерм - зависимостей количества адсорбированного вещества от его концентрации в растворе и нахождении величины адсорбции, соответствующей емкости монослоя. [11]
С целью определения зависимости R от концентрации ингибитора нами в данной работе были сняты изотермы адсорбции в широком диапазоне концентраций, для описания изотерм адсорбции обычно используют уравнения изотерм Ленгисра, Темкина, Фрейндлиха, Фрумкина и др., описанные в работах [ 4 51 /, которые устанавливают зависимость количества адсорбированного вещества от его концентрации. [12]
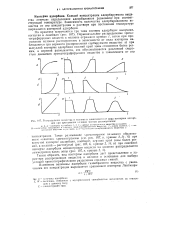 |
Распределение вещества в колонке в зависимости от вида изотермы адсорбции при промывании колонки чистым растворителем. [13] |
Каждой концентрации адсорбируемого вещества отвечает определенное адсорбционное равновесие при соответствующей температуре. Зависимость количества адсорбированного вещества от его концентрации в растворе при постоянной температуре выражается изотермой адсорбции. [14]
Величина адсорбции зависит от температуры, поверхности адсорбента, концентрации адсорбируемого вещества, химической и физической природы адсорбента и адсорбируемого вещества. Зависимость количества адсорбированного вещества из раствора от концентрации его в растворе при данной температуре называется изотермой адсорбции. [15]
Страницы: 1 2