Кислота
Cтраница 1
Кислоты получаются также при окислении метилкетонов или вторичных спиртов типа R - СП ( ОН) - СН3 гипогалогенитами. Хотя кислоты более высокого молекулярного веса, чем уксусная, обычно получаются с приемлемыми выходами при окислении олефиновых соединений хромовой кислотой, они все же не вполне устойчивы к действию окислителей. Так, при окислении стеариновой кислоты может получиться смесь низших кислот. Уксусная кислота, однако, совсем не взаимодействует с окислителями и часто применяется при окислении спиртов и алкенов в качестве растворителя. Более того, уксусная кислота почти всегда входит в состав продуктов окислительного расщепления в жестких условиях насыщенных и ненасыщенных соединений, содержащих метальные группы, связанные с углеродным атомом. Окисление проводят действием смеси хромовой и серной кислот, избыток реагента восстанавливают гидразином, реакционную смесь нейтрализуют щелочью и добавляют фосфорную кислоту. Уксусную кислоту отгоняют и определяют титрованием раствором щелочи. Природные соединения, содержащие группировку - СН2 - С ( СНз) СН - СН2 - , образуют один эквивалент уксусной кислоты из каждого такого звена. Как показывает анализ кислоты СНз - ( CH2) i6 - СООН по Куну - Роту, в ней присутствует одна ме-тильная группа ( концевая), в то время как в кислоте СН3 - ( СН2) 7 - СН ( СНз) - ( СН2) 8 - СООН найдены две С-метильные группы. При окислении гея-диметильной группировки при насыщенном атоме углерода - С ( СН3) 2 - не образуется уксусной кислоты. [1]
Кислоты всех этих типов растворимы в эфире. Натриевые и калиевые соли, будучи ионными, растворимы в воде и нерастворимы в эфире. Натриевые соли высших жирных кислот, обладая достаточной растворимостью в воде, применяются как поверхностно-активные мыла. [2]
Кислоты также претерпевают алкоголиз, сопровождающийся превращением гидроксильной группы в алкоксильную. [3]
Кислоты с удаленными от карбоксильной группы этиленовыми связями, начиная с винилуксусной СНа СН-СН2-СООН, обладают такой же способностью к реакциям присоединения, как и сами этиленовые углеводороды. Еще легче идут реакции присоединения, если этиленовая связь находится рядом с. [4]
Кислоты такого состава могут содержать или одну ацетиленовую или две этиленовые связи. [5]
Кислота C2iH4iCOOH и ее стереоизомер носят названия эруковой и брассидиновой кислот. [6]
Кислоты с удаленными от карбоксильной группы этиленовыми связями, начиная с винилуксусной СН2 СН-СН2-СООН, обладают такой же способностью к реакциям присоединения, как и сами этиленовые углеводороды. Еще легче идут реакции присоединения, если этиленовая связь находится рядом с карбоксильной группой ( а р-ненасыщенные кислоты), как в акриловой кислоте СН2 СН-СООН к ее гомологах. [7]
Кислоты такого состава могут содержать или одну ацетиленовую или две этиленовые связи. [8]
Кислоты и кислотоподобные вещества реагируют с основаниями по механизму донорно-акцепторного взаимодействия. [9]
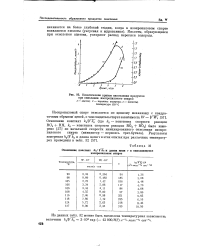 |
Кинетические кривые накопления продуктов. [10] |
Кислоты, образующиеся при окислении ацетона, ускоряют распад перекиси водорода. [11]
Кислоты, присоединяя молекулярный кислород по связям С - Н, образуют новую гидроперекись, в результате разложения которой образуются оксикислоты. [12]
Кислоты, растворенные в масле, действуют на такие металлы, как свинец и кадмий, только в присутствии другого окислителя. [13]
Кислоты, выделенные после окисления высокомолекулярных фракций нафтеновых углеводородов, представляют собой вязкие жидкости с уд. [14]
Кислоты, содержащие только карбоксильные группы, получаются при окислении масел разного молекулярного веса. [15]
Страницы: 1 2 3 4