Константа - скорость - обрыв - цепь
Cтраница 2
 |
Зависимость суммарной удельной скорости окисления от состава смеси ку-мол-этилбензол при различных температурах. [16] |
Здесь опять-таки основным действующим фактором является соотношение констант скоростей обрыва цепи А / А: - Ускорение наступает в результате роста концентрации радикалов. Константы скорости реакции продолжения цепи оказывают слабое влияние на ускорение процесса. [17]
Если обрыв цепей происходит в диффузионной области и константа скорости обрыва цепей может быть вычислена, из этих данных может быть найдена константа скорости продолжения цепи. [18]
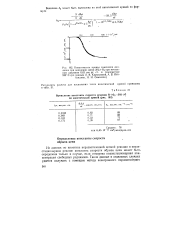 |
Кинетическая кривая изменения давления при окислении смеси 2Н2 Ог при начальном давлении 0 63 мм рт. ст. и температуре 522Э С ( по данным Л. В. Кармиловой, А. Б. Нал-бандяна, Н. Н. Семенова. [19] |
Из данных-по кинетике неразветвленной цепной реакции в квази-стащюнарном режиме константа скорости обрыва цепи может быть определена только в случае, если измерена квазистационарная кбн-центрация свободных радикалов. [20]
Возрастание значения этого параметра в случае ФМЭЦ обусловлено уменьшением величины константы скорости обрыва цепи. Этот эффект наблюдается также при введении в мономер объемного заместителя. [21]
Из данных по кинетике неразветвленной цепной реакции в квазистационарном режиме константу скорости обрыва цепи можно определить только при условии, если измерена квазистационарная концентрация свободных радикалов. Такие данные в отдельных случаях удается получить с помощью метода электронного парамагнитного резонанса. [22]
Так как в кинетической области ( / гг еш 2р) константа скорости обрыва цепи kr - 1 / р, а в диффузионной / ег - 1 / р2, для того, чтобы убедиться, что реакция протекает в диффузионной области, достаточно устано-вить зависимость скорости реакции от диаметра сосуда. [23]
Мы пока не делали никаких предположений о т, допуская, что константа скорости обрыва цепи kf не зависит от длины цепочки. Это не вполне очевидное предположение было сделано Флори [15] на следующих основаниях: акт обрыва кинетической цепи состоит из сближения двух цепочек ( если обрыв происходит за счет модификатора, постоянство kt не нуждается в доказательствах) и их взаимодействия, на которое требуется некоторое время. В целом это процесс диффузионно-управляемый. Но так как коэффициент диффузии коротких цепей больше, чем длинных, то, хотя короткие цепи быстрее сближаются, для них повышена вероятность того, что они разойдутся, не успев прореагировать. Длинные же цепи, напротив, сближаются медленно, но зато и вероятность того, что они разойдутся, не успев прореагировать, меньше. Поэтому сте-рические факторы констант скорости обрыва длинных и коротких цепей должны быть одинаковы. Что же касается энергий активации, то они определяются только природой взаимодействующих активных центров. При этом совершенно безразлично, какова детальная природа полимеризационного процесса - радикальная или каталитическая полимеризация или поликонденсация. [24]
В этом же параграфе будут описаны некоторые методы вычисления и экспериментального определения констант скоростей обрыва цепей. В тех случаях, когда могут быть использованы эти методы, они в сочетании с описанным методом определения отношений kjk3 или kick s позволяют определить абсолютные значения константы скорости лимитирующей стадии продолжения цепи. [25]
В то же время энергии активации реакций обрыва цепей обычно близки к нулю и константы скорости обрыва цепей мало зависят от природы свободного радикала. [26]
В случае радикальной полимеризации т - 1 / &3, где / с3 - константа скорости обрыва цепи, и средняя ( среднечисленная) степень полимеризации Рп определяется отношением kz / ka, где А: 2 - константа скорости роста цепи. В нашем случае мы также можем считать, что Рп / ( т, г), где v - скорость роста, но вид функции / ( т, v) будет уже гораздо сложнее, так как параметры т и v теперь определяются свойствами тройной системы мономер - катализатор - растворитель. Все средние веса выражаются формулами вида Mq - М0ехр ( а 32), где а - простой численный коэффициент, определяемый порядком - среднего веса [ 6; 2, стр. [27]
Весьма важным фактом, установленным в работе Николсона и Норриша [104], является уменьшение константы скорости обрыва цепей с увеличением давления. Авторы считают, что это уменьшение обусловлено ростом вязкости стирола с повышением давления. При этом существенно, что реакция продолжения цепей характеризуется константой скорости, которая в 106 раз меньше константы скорости обрыва цепей; этим и объясняется то обстоятельство, что реакция продолжения цепей, в отличие от их обрыва, протекает, как правило, в кинетической, а не в диффузионной области. [28]
Оцените эффективное значение константы скорости обрыва цепи при 25 % - ной конверсии, если начальная константа скорости обрыва цепи k0 2 6 107 л моль 1 -с 1, а остальные кинетические константы и эффективность инициирования в указанном интервале превращений не меняются. [29]
В то же время энергии активации реакций обрыва цепей обычно близки к нулю, и поэтому константы скорости обрыва цепей мало зависят от природы свободного радикала. Поэтому отношение скоростей гибели цепи на различных свободных радикалах wT1 / wr2 определяется в первую очередь отношением концентраций этих свободных радикалов и, следовательно, как правило, сильно отличается от единицы. [30]
Страницы: 1 2 3 4