Константа - скорость - термическое разложение
Cтраница 1
Константы скорости термического разложения в растворах жирных кислот в зависимости от величины цикла увеличиваются в следующем ряду: 5 -, 6 -, 15 -, 7 - и 8-членные циклические мочевины. Как и следовало ожидать, разложение замещенных мочевин в растворах в карбоновых кислотах зависит от природы и кислотности применяемой кислоты. Авторы также отметили, что скорость выделения углекислого газа имеет первый порядок по концентрации замещенной мочевины и для арилзамещенных мочевин она выше, чем для силш-диметилмочевины. Сама мочевина в этих условиях реагирует по реакцди второго порядка. [1]
Сравнение величин константы скорости термического разложения показывает, что как в случае диацилперекисей, так и в случае перэфиров скорость термического разложения резко возрастает при увеличении степени замещения углеродного атома, непосредственно связанного с карбоксигруппой. [2]
Сравнение величин константы скорости термического разложения показывает, что как в случае диацилперекисей, так и в случае перэфиров скорость термического разложения резко возрастает при увеличении степени замещения углеродного атома, непосредственно связанного с карбоксигруппой. Соответственно наблюдается понижение величины энергии активации реакции термического разложения. [3]
 |
Термическое разложение диацилперекисей в стироле. [4] |
Численные значения констант скорости термического разложения изученных перекисей в стироле, определенные с помощью ИК-спектроскопии, оказались выше значений констант, найденных ранееш для разложения тех же перекисей в этилбензоле. [5]
 |
Термическое разложение диацилперекисей в стироле. [6] |
Численные значения констант скорости термического разложения изученных перекисей в стироле, определенные с помощью ИК-спектроскопии, оказались выше значений констант, найденных ранее10 для разложения тех же перекисей в этилбензоле. [7]
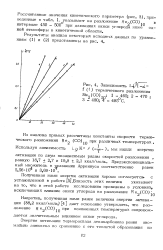 |
Зависимость 1 - ( / 1-о ( f ( t термического разложения Re ( СО 1 - 465. 2 - 470 3 - 480. [8] |
Из наклона прямых рассчитаны константы скорости термического разложения Re ( СО) 1П при различных температурах. [9]
В основу расчета положены константы скоростей термического разложения метана, этана, этилена и ацетилена, полученные Г. И. Козловым и В. Г. Кнорре [11] в экспериментах на ударной трубе. Эти данные удовлетворительно согласуются с данными других авторов [12-17] ( рис. 3), но, в отличие от них, получены в области более высоких температур. Исключение составляет константа скорости разложения ацетилена. [10]
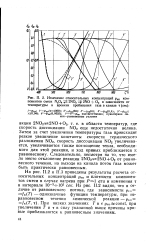 |
Изменение относительных концентраций рко компонентов смеси N2O4 2NO2 z. 2NO О2 в зависимости от температуры и времени пребывания газа в канале т ( сек. [11] |
Затем за счет увеличения температуры газа происходит резкое увеличение константы скорости термического разложения NO2, скорость диссоциации NO2 увеличивается, увеличивается также поглощение тепла, необходимого для этой реакции, и ход кривых приближается к равновесному. Следовательно, несмотря на то, что имело место отклонение реакции 2NO25 2NO O2 от равновесного течения, на выходе из канала поток газа может быть практически равновесным. [12]
Она становится существенной в области повышенной концентрации реагирующих веществ и проявляется в увеличении константы скорости термического разложения инициатора с повышением его концентрации. Наблюдающаяся в этих условиях валовая скорость разложения инициатора представляет собой суммарное выражение термического и индуцированного распада. [13]
Термическое разложение ацетона происходит при 578 К на 25 % за 90 9 с, пзи 601 К - за 31 с. Рассчитайте константу скорости мономолекулярного термического разложения а цетона, энергию активации этого процесса и расход энергии элект-ромагнитного излучения ( Дж / моль) в фотохимическом процессе. [14]
С увеличением дозы облучения ультрафиолетовым светом константа скорости термического разложения быстро возрастала до постоянного значения, которое было больше для растертых, чем для целых кристаллов. Описанные Марке результаты удалось воспроизвести только после добавления к азиду кальция переходных металлов. Следовательно, процесс образования ядер, идущий во времени, обусловлен наличием примесей. Другим важным результатом было наблюдение резкого возрастания ( на несколько порядков) электропроводности таблетки разлагающегося азида кальция в момент, соответствующий точке перегиба кинетической кривой. Это говорит об образовании плотных объемных ядер. [15]
Страницы: 1 2