Константа - скорость - реакция - обмен
Cтраница 1
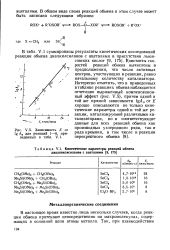 |
Зависимость Е от lg А0 для реакций 1 - 6, приведенных в V. 1.| Кинетические параметры реакции обмена диалкоксисиланов с ацеталями. [1] |
Константы скоростей реакций обмена вычислены в предположении, что число активных центров, участвующих в реакции, равно начальному количеству катализатора. [2]
На рис. 21 приведены зависимости констант скоростей реакций обмена, рассчитанных с помощью этих кривых для систем D2 - Н2О и HD - Н2О, от концентрации иона гидроксила. Самая верхняя кривая относится к конверсии параводорода, которая, следовательно, протекает несколько быстрее, чем реакция обмена. [3]
Соотношение (4.16), определяющее величину константы скорости реакции обмена электрона, явно выражает возможность конкуренции между двумя путями реакции: легким, когда вследствие большого расстояния между ионами энергия отталкивания реагентов невелика, но в то же время мала вероятность туннельного перехода электрона; и трудным, когда реакция происходит при тесном сближении реагентов, при этом % е близка к единице, однако велика энергия отталкивания. При некотором определенном значении гаь эти две тенденции оказываются сбалансированными и тогда скорость обмена становится максимальной. [4]
На основе экспериментальных данных по константам скорости реакций обмена построены LEPS-поверхности потенциальной энергии для рассматриваемых взаимодействий. [6]
Задача 6.13. В приближении МПС вычислить константу скорости реакции обмена А ВС - АВ С в предположении, что линейный активированный комплекс ABC отвечает положению системы на вершине потенциального барьера. [7]
 |
Параметры построенных LEPS-поверхностей потенциальной энергии. [8] |
Гр - рассчитанное методом классических траекторий, a k - экспериментальное [89] значение константы скорости реакций обмена: Т 2000 К, 7 2 2500 К, Г3 3000 К. [9]
Эффективная константа устойчивости комплекса, образованного анализируемым металлом со свободным ли-гандом, определяет будет ли металл заметно уменьшать константу скорости реакций обмена. Если концентрация свободного лиганда равна 10 - 8 - 10 - 6 моль / л, то комплексное соединение с анализируемым металлом должно иметь большую константу устойчивости, иначе металл не будет полностью закомплексован, и поэтому определение не будет чувствительным. Изменяя рН, можно превращать многие металлы в формы, удобные или неудобные для определения. Следовательно, селективность метода можно повысить, изменяя рН и используя маскирующие вещества. [10]
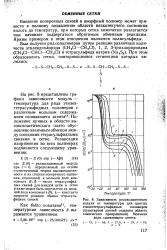 |
Зависимость релаксационного модуля от температуры для сшитых этилентетрасульфидных полимеров ( пунктирной линией отделена область химических превращений. Мольная Доля сшивающего агента. [11] |
В, Р - число тетрасульфид-ных связей для каждой цепи в сетке ( также может быть определено из мольной доли компонента В); k - константа скорости реакции обмена тетрасуль-фидных связей. [12]
Было обнаружено, что скорость обмена водорода, находящегося в орто-положении замещенного бензола, сильно зависит от электроотрицательности групп заместителя. Так, константа скорости реакции обмена для фторбензола более чем в 107 раз превышает константу скорости реакции с толуол ом. [13]
Изменения Е и IgA для обмена йода между 2 4-динитройодбензолом и йод-ионами ( см. табл. 2) значительно больше и, возможно, могут быть связаны с большим объемом, на который распространяется заряд в переходном состоянии в случае ароматического нуклеофильного замещения. С другой стороны, константа скорости реакции обмена метоксильных групп в метаноле ( табл. 3) дает мало доказательств действия солевого эффекта, хотя значения для 0 0023 М раствора метоксильных ионов лежат несколько выше графика Арре-ниуса. Бамфорд ( Bamford) [4] изучал нуклеофильное замещение нитрогруппы метоксильной группой в метанольном растворе в серии динитробензолов и динитронафталинов и ни в одном случае не нашел доказательств солевого эффекта этого типа. Возможно, что распространение заряда в переходном состоянии при включении метоксильного иона происходит значительно в меньшей степени; поведение йодида калия и метилата натрия как электролитов в ацетоне и метаноле соответственно в некоторых отношениях различно. Ясно, что требуется значительно больше экспериментальных данных прежде, чем объяснение этого типа солевого эффекта может быть дано с какой-либо достоверностью. [14]
По существу предложенный метод заключается в титровании ингибиторов ионами металлов с определением нескольких скоростей реакции при добавлении известного количества EDTA к неизвестному количеству никеля. Этот метод аналогичен амперометрическо-му титрованию, константа скорости реакции обмена аналогична току. [15]
Страницы: 1 2