Константа - скорость - реакция - первый порядок
Cтраница 1
Константа скорости реакции первого порядка не зависит от способа выражения концентрации. [1]
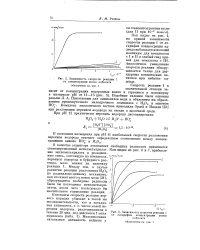 |
Зависимость скорости реакции 1 от концентрации ионов кобальта.| Зависимость скорости реакции 1. [2] |
Константы скорости реакции первого порядка убывают в такой же последовательности, что и каталаз - о ная активность, т.е. число молей перекиси водорода, разложившихся в течение 20 мин. [3]
Константа скорости реакции первого порядка с достаточной точностью описывает разложение обеих применявшихся сырьевых смесей, значительно различавшихся по величине парциального давления метана. Хотя возможное торможение разложения метана водородом непосредственно не исследовалось, но было обнаружено, что относительные выходы продуктов изменяются во времени при данной температуре пиролиза, несмотря на постоянство скорости разложения метана. Как указывают авторы [54], это означает, что продукты разложения лишь незначительно влияют на разложение метана. При экстраполяции кривой Аррениуса для сравнения с результатами исследований, проводившихся в кварцевом и фарфоровом реакторах в области более низких температур, было обнаружено, что в последнем случае получаются более высокие скорости реакции, но меньшие значения энергии активации. Это позволяет предположить протекание гетерогенных каталитических реакций, причем роль катализатора играют или стенки реактора, или углерод, образующийся в ходе реакции. [4]
Константы скоростей реакций первого порядка интерпретируются при таком подходе как линейные эффекты bj, константы скоростей смешанного второго порядка - как эффекты взаимодействия buj и константы скоростей реакции второго порядка - как квадратичные эффекты - Ьц. Если схема реакций заранее неизвестна, но известны все те вещества, которые могут участвовать в реакции, то план эксперимента составляется таким образом, чтобы по результатам опытов можно было найти независимые оценки всех коэффициентов полиномов второго порядка. Далее проводится проверка значимости коэффициентов и определяется схема реакции. [5]
Константа скорости реакции первого порядка, отнесенная к единице площади поверхности. [6]
Константы скоростей реакций первого порядка интерпретируются при таком подходе как линейные эффекты bj, константы скоростей смешанного второго порядка - как эффекты взаимодействия buj и константы скоростей. Если схема реакций заранее неизвестна, но известны все те вещества, которые могут участвовать в реакции, то план эксперимента составляется таким образом, чтобы по результатам опытов можно было найти независимые оценки всех коэффициентов полиномов второго порядка. Далее проводится проверка значимости коэффициентов и определяется схема реакции. [7]
Константа скорости реакции первого порядка равна 2 5 - 107 сек-1, я исходная концентрация составляет 0 1 кмоль: мл. [8]
Константа скорости реакции первого порядка равна 4.02 - Ю-4 с 1 при 393 К и 1.98 - 1 0 3 с 1 при 413 К. [9]
Константа скорости реакции первого порядка газофазного разложения вещества X равна 2 0 - КНс 1 при 300 С. [10]
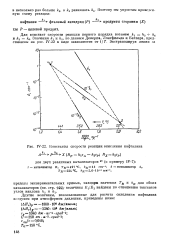 |
Константы скорости реакции окисления нафталина fci k. [11] |
Для констант скорости реакции первого порядка возьмем Ах k3 A4 и &2 e - Значения k: и k2, по данным Демериа, Лонгфильда и Батлера, представлены на рис. IV-22 в виде зависимости от. [12]
Если известна константа скорости реакции первого порядка и начальная концентрация, то можно вычислить концентрацию в любой момент времени. [13]
Какова размерность константы скорости реакции первого порядка и в каких единицах измеряется константа скорости. [14]
Введем три константы скорости реакции первого порядка k0, kit kz, которые отвечают вероятности реакции в единицу времени, отнесенной к одному свободному звену, если это звено имеет рядом с собой соответственно О, 1 или 2 занятых звена. Как уже отмечалось, будем считать, что молекулы достаточно длинные, таким образом, можно не рассматривать эффектов, связанных с их концами. [15]
Страницы: 1 2 3 4