Константа - скорость - прямая реакция
Cтраница 2
 |
Зависимость равновесного. [16] |
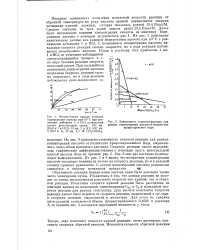
Температурная зависимость константы скорости прямой реакции соответствует энергии активации Е - 100 кДж / моль. [17]
С повышением температуры константа скорости прямой реакции во всех случаях возрастает, причем более резко, чем по уравнению Фроста. [18]
Для таких процессов константа скорости прямой реакции kl с возрастанием температуры увеличивается медленнее, чем константа скорости обратной реакции Ла. Это свидетельствует о том, что величина - WA достигает при дайной температуре максимального значения. [19]
С повышением температуры константа скорости прямой реакции во всех случаях возрастает, причем более резко, чем по уравнению Фроста. [20]
В приведенных соотношениях константы скоростей прямых реакций приняты равными единице. [21]
Теперь, зная константу скорости прямой реакции, легко рассчитать константу скорости обратной реакции. [23]
Если при данной температуре константа скорости прямой реакции имеет большее значение, чем константа скорости обратной, то какая из них будет экзотермической. [24]
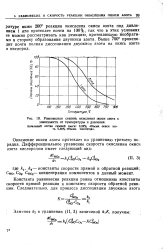 |
Равновесная степень окисления окиси азота в зависимости от температуры и давления. [25] |
Константа равновесия реакции равна отношению константы скорости прямой реакции к константе скорости обратной реакции. [26]
В этих равенствах k обозначает константу скорости прямой реакции, a k2 - константу скорости обратной реакции. [27]
Коэффициент пропорциональности / q называется константой скорости прямой реакции, а выражения в квадратных скобках [ N2 ] и [ О2 ] означают молярные концентрации в молях на литр. [28]
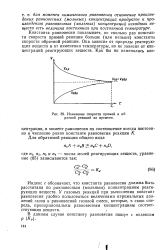 |
Изменение скорости прямой и обратной реакций во времени. [29] |
Константа равновесия показывает, во сколько раз константа скорости прямой реакции больше ( или меньше) константы скорости обратной реакции. Она зависит от природы реагирующих веществ и от изменения температуры, но не зависит от концентраций реагирующих веществ. [30]
Страницы: 1 2 3 4 5