Константа - стабильность
Cтраница 3
Предложены электроды с твердым внутренним контактом - графитовым стержнем ( так называемые селектроды) на основе различных препаратов Си2 1: CuS, CuS - Ag2S, CuS - HgS. В работе [247] этот электрод применен для определения констант стабильности комплексов Си2 с глицином и ЭДТА. [31]
Последнее соотношение было использовано Купером и др. [173] при сравнении характеристик комплексообразования, определенных хроматографическим и спектральным методами. Генкин [175] применил эту же зависимость для определения констант стабильности комплексов, значения у были получены в результате хроматографического эксперимента, а у - расчетным методом. [32]
В случае ферментативной системы наибольшая константа стабильности ( получена для комплекса Е - ПГ. Предположим, что в результате связывания флавина с белком не изменится соотношение констант стабильности комплексов ПГ с флавином в окисленном и полувосстановлежном состоянии. [33]
Предложены и приведены новые методы для измерения констант ионизации летучих органических веществ и констант стабильности комплексов металлов с ненасыщенными и ароматическими углеводородами. [34]
Взаимодействие углеводородов с поли / хром ( Ш) дифенилфосфинат / ом; расчет констант стабильности - комплексов в газовой адсорбционной хроматографии. [35]
Степень проч-тости комплексов металлов с ЭДТУ в свою очередь коррелирует со способностью металлов образовывать комплексы с такими биологически важными образованиями, как белки, ферменты, субстраты клеточных оболочек. Токсичность таких сильных ядов, как ртуть, кадмий, индий, линейно возрастает с увеличением их константы стабильности в комплексах с ЭДТУ, а также с прочностью их сульфидов. [36]
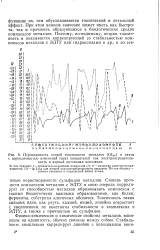 |
Периодичность острой токсичности металлов ( DLSO в связи с периодичностью изменений таких показателей как электроотрицательность и первый потенциал ионизации. [37] |
Степень прочисти комплексов металлов с ЭДТУ в свою очередь коррелирует со способностью металлов образовывать комплексы с такими биологически важными образованиями, как белки, ферменты, субстраты клеточных оболочек. Токсичность таких сильных ядов, как ртуть, кадмий, индий, линейно возрастает с увеличением их константы стабильности в комплексах с ЭДТУ, а также с прочностью их сульфидов. [38]
Описанные выше корреляции могут быть использованы не только при исследованиях металлсодержащих ферментов и комплексов металлов с макромолекулами. Например, исследование констант активации или ингибирования какой-либо ферментативной реакции ионами различных металлов и сравнение этих констант с константами стабильности комплексов тех же ионов с различными лигандами может дать представление о природе групп активного центра фермента. Всевозможные сравнительные исследования ионов металлов чрезвычайно полезны для изучения специфических участков крупных молекул. [39]
При рН 7 уксусная и щавелевая кислоты и до известной степени имидазол представлены их константами образования, но у всех других лигандов на фиг. При возрастании рН на единицу рМ также возрастает на единицу, и так до тех пор, пока рМ не достигнет величины логарифма константы стабильности для данного лиганда, после чего дальнейшее возрастание прекращается. При изменении рН в другом направлении, в сторону повышения кислотности до величин рН 5, точки, соответствующие всем лигандам, за исключением уксусной и щавелевой кислот, смещаются вверх; при этом уменьшению рН на единицу также соответствует смещение точки на единицу по оси ординат. При рН, меньших 5 5, величина рКа уксусной и щавелевой кислот становится значительной, поскольку при этих условиях значительная часть всей кислоты находится в протони-зированной форме. [40]
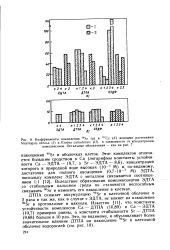 |
Коэффициенты накопления 90Sr ( а и 137Cs ( б водными растениями. [41] |
ДТПА снижает аккумуляцию 90Sr в клеточной оболочке в 2 раза и так же, как в случае с ЭДТА, не влияет на накопление 90Sr в протоплазме и вакуоли. Известно [11], что константы устойчивости комплексов Са - ДТПА ( 10 89) и Са - ЭДТА ( 10 7) примерно равны, а константа стабильности Sr - ДТПА ( 9 68) больше в 10 раз. [42]
Принципы, использованные при определении групп, образующих координационные связи в цистеинате цинка, могут быть применены для аналогичных целей и в случае белков. Карбок-сипептидаза А - протеолитический металлсодержащий фермент - имеет в своем активном центре ион цинка, который может быть замещен различными двухвалентными ионами переходных металлов. Константы стабильности комплексов всех этих ионов с белком были определены. [43]
Комплеисообразование изучалось спектрофотометрически по, отклонению системы от закона Ламберта - Беера. Оказалось, что ПГ образует комплексы с окисленной, восстановленной и полувосстановленной формами ФМН. Полученные значения констант стабильности комплексов для двух значений рН среды приведены ниже. [44]
Различные металлы образуют предпочтительно ту или другую из этих трех структур в соответствии с указанными ранее принципами. Первая структура с шестичленным хелатным кольцом встречается реже, чем две последние, которые имеют лишь по пять атомов в хелатном кольце. Обратившись к табл. 19, в которой приведены константы стабильности подобных соединений, можно установить, какая из структур должна преобладать. Удобными модельными соединениями, образующими хелатные комплексы, подобные этим трем структурам, являются меркап-топропиойовая кислота, глицин и 2-меркаптоэтиламин. Для иона цинка логарифмы первых констант образования этих структур равны 6 8, 5 5 и 9 9 соответственно. Поскольку лишь третья структура имеет константу образования, близкую к константе для цистеината цинка, можно сделать вывод, что образование хелата в подавляющем большинстве случаев происходит с участием донорных атомов N и S. [45]
Страницы: 1 2 3 4