Энергетическая константа
Cтраница 1
Энергетическая константа, аналогичная еж, впервые была введена в физическую химию В. [1]
Энергетическая константа в уравнении Ленгмюра зависит как от природы глины, так и от обменного катиона. Наибольшее значение эта константа имеет при сорбции Ш2 - ионов, а наименьшее - при сорбции Cd2 - ионов. Известно, что при обмене ионов с одинаковым зарядом обмен данного иона тем больше, чем меньше его ионный радиус. Значение константы b при сорбции на А1 - форме глины на порядок ниже, чем соответствующее значение для Н - формы; следовательно, связь обменных А1 - ионов с поверхностью глины значительно сильнее, чем связь водородных ионов, и поэтому вытеснение алюминия кадмием, кобальтом и никелем затруднено. [3]
Энергетические константы, предложенные А. Е. Ферсманом, и новая формула А. Ф. Капустинского для расчета энергии кристаллов. [4]
К - энергетическая константа, характеризующая данную систему адсорбент - адсорбат - растворитель. При п 1 вместо прямой получается кривая, вогнутая по отношению к оси абсцисс; при п 3 - выпуклая. [5]
С помощью описанных энергетических констант легко вычислить приблизительные значения энергии решеток различных соединений и использовать их при анализе ряда геохимических процессов. В табл. 18 приводятся значения эк ов и взк ов некоторых ионов. [6]
В теории Андерсона взаимодействие дефектов учитывается введением энергетической константы ЕНн ( или Ец), а концентрационная зависимость энергии взаимодействия дефектов учитывается исключительно умножением этой константы на число пар ближайших соседних дефектов, которое вычисляется в приближении хаотического распределения дефектов. [7]
Функция / ( 0) состоит из следующих энергетических констант: ст12, а13, ст23 - свободная энергия единичной поверхности раздела соответственно глина - металл трубы, глина - жидкая фаза бурового раствора и металл трубы - жидкая фаза бурового раствора. [8]
Большой интерес представляет обнаруженное изменение величины Х - энергетической константы, характеризующей состояние иона в той или иной группе соединений. Как следует из рис. 35, значение Х, соответствующее наибольшей степени ионизации серы в решетках типа NaCl, на 3 3 X меньше величины Хдо, отражающей особенности энергетического состояния серы в соединениях с решетками типа NiAs и ZnS. В этих последних поляризация серы много сильнее, и связь в значительно меньшей степени может считаться чисто ионной, чем в соединениях с решетками типа NaCl. Таким образом, соотношения ( 38) и ( 39) действительно передают общие закономерности, связывающие длину волны основного края поглощения атомов с основными параметрами соединения: междуатомным расстоянием в решетке и степенью поляризации составляющих ее ионов. Более того, сгруппировав рассматриваемые соединения по принципу принадлежности их к одному типу кристаллической решетки при одинаковой валентности изучаемых ионов, возможно сделать некоторые выводы об особенностях энергетического состояния данных ионов в соединениях. Эти выводы вполне согласуются с результатами исследования указанных веществ другими методами. [9]
 |
Значения a ] / Р некоторых материалов для нитей катарометров. [10] |
К) - константа, характерная для каждого вещества, называемая энергетической константой; Т ( К) - температура сопротивления. Сопротивление при 20 С составляет в обоих случаях 10 ком. [11]
На рис. 71 приведен типичный вид такой зависимости, построенной в [6] по заданным значениям энергетических констант. [12]
АФМР ио ( Ну) для ортоферритов в состоянии с / Н У, для которых пригоден эффективный термодинамический потенциал вида (6.100), учитывающий взаимодействие ионов Fe и R путем перенормировки его энергетических констант. В частности, речь может идти об ортоферрите диспрозия DyFeOs при температурах ниже точки Морина TM 50 К. К сожалению, соответствующие экспериментальные данные в поле Ну ф 0 авторам неизвестны. [13]
 |
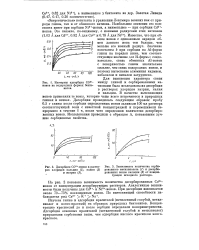
Зависимость молекулярных площадей от константы СБЭТ для азота, аргона и криптона. [14] |
Как указывалось, плотность упаковки молекул зависит в первую очередь от энергии адсорбции и величины оот антибатны этой энергии. Некоторое представление об этой зависимости можно получить из сопоставления значений ит энергетической константой С вэт как это было сделано впервые Киселевым ж Эльтековым [9] для w - пентана. На рис. 7 представлена зависимость чт-от СБЭТ для изученных трех адсорбатов. Конечно, приведенные кривые дают лишь качественное представление об этой зависимости. Весьма желательно прямое сопоставление от-с величинами калориметрически определенных теплот. В [ 101 высказана идея о зависимости ит от степени локализации адсорбированных молекул, которая, в свою очередь, также должна зависеть от энергии адсорбции. [15]
Страницы: 1 2