Условная константа - скорость
Cтраница 1
Условная константа скорости учитывает влияние среды, концентрации различных ионов, температуры на скорость реакции и в общем случае является сложной функцией этих параметров. [1]
Условная константа скорости реакции К зависит, вообще говоря, от температуры, при которой протекает реакция. Поэтому должно быть учтено также распределение температуры по длине печи. [2]
Условные константы скорости реакций были определены по экспериментальным данным, характеризующим один из установившихся режимов, после чего расчетные результаты дали хорошее совпадение с экспериментальными для всех прочих исследованных режимов. [3]
Сравнение условной константы скорости каталитической реакции при оптимальной концентрации Н2О2 ( k 7200 200) М-1-мин-1 с константами скоростей реакции прямого взаимодействия хромат-иона с ОАФ ( fe 70 10) М - - мин-л и хромат-иона с HgCb ( k 120 20) М-1-мин-1 показало, что реакции прямого взаимодействия Cr ( VI) OAO и Cr ( VI) - j - Н2С2 не могут быть скоростьопределяющими для каталитической реакции. По-видимому, эти процессы приводят к дезактивации хромат-иона в ходе каталитической реакции, вследствие чего кинетическая кривая каталитической реакции имеет заметный изгиб при времени реакции более 6 - 10 минут. [4]
Здесь k - условная константа скорости, величина которой зависит от концентрации реагирующих веществ X и R, взятых в избытке. [5]
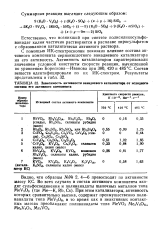
Наибольшие значения величин условных констант скоростей каталитических реакций получены для реакций окисления n - фенилендиамина и его смеси с о-изомером, а также при окислении 1 -амино - 2-нафтол - 4-сульфокислоты. [6]
При увеличении температуры растворов условная константа скорости реакции ( [ Н2О2 ] 2 8 10 - 3 М; [ Fe ] 3 58 - 10 - 6 М; [ НМОз ] 0 01 М) увеличивается. [7]
Определен порядок и вычислены условные константы скорости гидролиза. [8]
Это видно из сравнения условных констант скоростей реакции Аусл, приведенных ниже. [9]
К - постоянная, представляющая собой произведение условной константы скорости, молярного коэффициента погашения индикаторного вещества и толщины кюветы. [10]
Выделены три зоны с различным характером протекания гидролитических процессов и вычислены условные константы скорости гидролиза. [11]
Скорость реакции ДСи / Ar в сответствии с кинетическим уравнением пропорциональна условной константе скорости k и зависит от концентрации реагентов. В свою очередь константа k зависит от температуры, ионной силы и рН раствора. Таким образом, величина Ъ определяется природой реагентов и условиями проведения реакции, а также методом измерения скорости. [12]
Экспериментальные данные, полученные в условиях проведения опытов ( табл. 2), были использованы для определения условных констант скорости реакции К. [13]
Каталитическое алкилирование, повидимому, является параллельно-последовательной реакцией 2-го порядка, переходящей при больших избытках изобутана в псевдомономолекулярный консекутивный процесс. Условные константы скоростей реакций, включающие в себя поверхность раздела жидкостей, должны быть прямо пропорциональны достигнутой степени эмульгирования исходных продуктов и катализатора. [14]
 |
Зависимость активности ванадиевого катализатора от исходного состава его активного компонента. [15] |
Страницы: 1 2