Копланарность
Cтраница 1
Копланарность, В бифеннле наиболее существенную роль играет резонанс между структурами Ке-куле в каждом отдельном кольце. Но можно еще написать менее стабильные структуры, которые представлены в заметной, хотя и небольшой степени. [1]
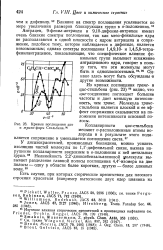 |
Кривые поглощения цис и транс-форм Стильбена. 96. [2] |
Копланарности г с-стильбена мешают о-расположенные атомы водорода и в результате этого подавляется сопряжение и уменьшается поглощение света. [3]
Копланарность ароматического кольца и гидроксильной группы ( связи С-О) подтверждается также следующим расчетом, выполненным К. Известно, что основная частота колебаний карбонильной группы различных замещенных бензальдеги-дов находится в прямой зависимости от о пара-заместителя. [4]
Копланарность стабильных свободных радикалов подтверждается отсутствием у них оптич. [5]
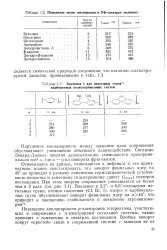 |
Положение полос поглощения в УФ-спектрах полиенов.| Значения А для некоторых типов31 карбоцепных полисопряженных систем. [6] |
Нарушение копланарности между звеньями цепи сопряжения обусловливает уменьшение обменного взаимодействия. Согласно Ленард-Джонсу энергия делокализации уменьшается пропорционально cos2 а, где а - угол поворота фрагментов. [7]
Гипотеза копланарности подтверждается исследованием замещенных производных бензидина. Было установлено, что только те производные бензидина дают субстантивные красители, которые содержат заместители в 3 3 -положениях; 2 2 -замещенные бензидина не дают субстантивных красителей. [8]
Нарушение копланарности в результате выведения нитрогруппы из плоскости бензольного кольца должно затруднить энергетически выгодное я-сопряжение в р-нитростиролах и в а-фурил-р-нитро - этилене и приблизить их моменты к моментам алифатических нитросоединений, что не имеет места. Следовательно, предположение о некопланарности исследованных веществ также отпадает. [9]
Нарушение копланарности не Связано только с поворотом вокруг единичной связи С-С в бутадиеновой системе, так как в этом случае коэффициенты интенсивности в исследованных ( Va и V6) и модельном соединениях ( IV) были бы одинаковы. [10]
Отсутствие копланарности может быть вызвано стерическими причинами. Так, при введении двух метильных групп в орго, opro - положения диметиланилина происходит увеличение утла между осью орбитали неподеленной пары электронов и осями р-электронов бензольного ядра от 31 39 до 6Г355 [ 51, 1977, с. Это приводит к значительному уменьшению дипольного момента. [11]
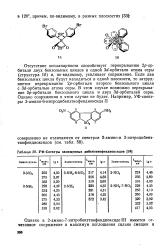 |
УФ-Спектры замещенных дибензтвофендиоксидов. [12] |
Отсутствие копланарности способствует перекрыванию 2р - ор-битали двух бензольных циклов и одной Зс. Если два бензольных цикла будут находиться в одной плоскости, то затрудняется перекрывание 2р - орбитали второго бензольного цикла с Sd-орбиталью атома серы. В этом случае возможно перекрывание 2 / 7-орбитали бензольного цикла и двух Sd-орбиталей серы. [13]
Условие копланарности связано с необходимостью максимального перекрывания р-орбиталей. [14]
Ваюушение копланарности в результате выведения нитрогруппы из плоскости бензольного кольца должно затруднить энергетически выгодное Д - сопряжение в - нитростиролах и приблизить их моменты к моментам алифатических китросоединений, что не имеет места. [15]
Страницы: 1 2 3 4