Кривая - катодная поляризация
Cтраница 1
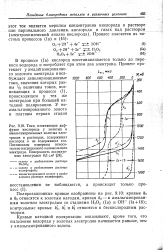
Кривая катодной поляризации / пересекается с кривой анод ной поляризации 1 на участке, характеризующем ионизацию металлов при потенциале более отрицательном, чем значение первой. Зашита металла в этих условиях может быть обеспечена увеличением окислительно-восстановительного потенциала среды до значений, превышающих значение первого критического анодного потенциала Е к, что может быть достигнуто увеличением концентрации окислителя или введением в раствор окислителя с более высоким окислительно-восстановительным по тенциалом ( фиг. В этом случае кривая катодной поляризации 2 пересекает анодную кривую на участке, характеризующем пассивное состояние металла. [1]
Кривые катодной поляризации показывают, кроме того, что выделение водорода у золотых электродов начинается раньше, чем у амальгамированного золота. [3]
Кривые катодной поляризации при 30 кгц на несколько мом см2 отличаются от значений при других частотах. [4]
Кривые катодной поляризации имеют три ветви. [5]
Кривые катодной поляризации различных рН; температура 60 20 мв; при содержании 20г / л Н 1В03 и плотности тока 200 а / м2 катодная поляризация повышается на 75 мв. [6]
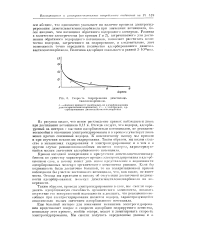 |
Скорость гидрирования дгшетилаце-тиленилкарбипола. [7] |
Кривая катодной поляризации в присутствии диметилацетиленилкар-бинола по существу характеризует процесс электрогндриронапия в адсорбционном слое, а потому может дать ясное представление о подвижности адсорбированных молекул органического компонента реакции. Если бы подвижность была достаточно большой, то на поляризационной кривой наблюдался бы участок постоянного потенциала, что, как видно, не имеет места. Отсюда мы приходим к выводу об отсутствии достаточной подвижности адсорбированных молекул диметилацетиленилкарбпнола на поверхности. [8]
 |
Микроструктура покрытия Sn - Bi. [9] |
Кривые катодной поляризации ( рис. 107) при выделении сплава Sn - Zn подтверждают, что с увеличением содержания свободного цианида в электролите равновесный потенциал сплаво-образования смещается в сторону положительных значений. Это объясняется тем, что цинк в таком электролите находится в более прочных циа-нидных комплексах, и его соосаждение замедляется. [10]
Кривые катодной поляризации титана имеют три ветви. [11]
Кривая катодной поляризации титана в 0 5 % HF имеет форму прямой ( фиг. И) и по-видимому не отражает истинного характера катодных процессов на поверхности металла. [12]
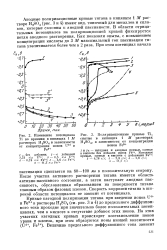 |
Изменение потенциала Ti во времени в кипящих 1 М растворах H2S04 в зависимости от концентрации ионов U6 и Fe3.| Поляризационные кривые Ti. [13] |
Кривые катодной поляризации титана при введении ионов U6 и Fe3 в растворы H2S04 ( см. рис. 3 и 4) до предельного диффузионного тока проходят при значительно более положительных потенциалах, чем в кислоте в отсутствие добавок этих ионов. [14]
Кривые катодной поляризации титана имеют три ветви. [15]
Страницы: 1 2 3 4 5