Кривая - катодная поляризация
Cтраница 2
 |
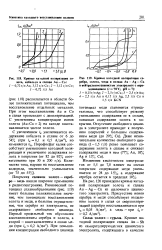
Поляризационные кривые, снятые соответственно при комнатной температуре и 60 С в электролитах, содержащих золото, г / л. / и / - 10. 2 и 2 - 25 и 3 и 3 - 40. [16] |
Кривые катодной поляризации ступенчатой формы, на них имеется несколько участков, соответствующих различным катодным процессам. [17]
Как показывают кривые катодной поляризации, резкое увеличение скорости коррозии в кислых средах вызвано облегчением катодной реакции восстановления водорода без изменения стационарных электродных потенциалов. В щелочной области повышение скорости коррозии сопровождается резким разбла-гораживанием потенциалов, что обусловлено растворением окисной пленки на поверхности сплава и переходом его в активное состояние. Коррозия металлов в сильно щелочных средах происходит за счет катодной реакции ионизации кислорода, поэтому потенциал активированной поверхности смещается в отрицательную сторону до тех пор, пока не будет достигнуто перенапряжение реакции выделения водорода из молекулы воды, соответствующее катодной плотности тока при данном значении рН среды. [18]
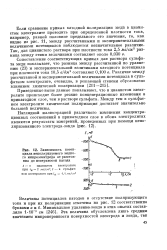 |
Зависимость потенциала неполяризуемого медного микроэлектрода от расстояния до поверхности катода. [19] |
Если сравнение кривых катодной поляризации меди в цианистом электролите проводить при определенной плотности тока, например, равной половине предельного его значения, то, как видно из рис. 11, между рассчитанными и экспериментальными величинами потенциалов наблюдается незначительное различие. [20]
Общий вид кривых катодной поляризации палладия в таких растворах приведен на рис. 71 ( см. стр. [21]
Эта кривая - кривая катодной поляризации катодных участков ( так называемая идеальная поляризационная кривая ], является характеристикой катодного процесса на данном материале, а при наличии аналогичной характеристики анодного процесса используется для построения коррозионных поляризационных диаграмм, являющихся графической характеристикой коррозионного процесса в аэрированном водном растворе. [22]
Полученная таким образом кривая катодной поляризации сравнивалась с обычной кривой катодной поляризации, полученной в отсутствие органического вещества. [23]
На основании анализа кривых катодной поляризации железа в 3 / 0-ном растворе NaCl без перемешивания Н. Д. Томатов определил оптимальную плотность тока к 0 01 а / дм-для нрокорродировавшей железно. [24]
 |
Примерная кривая катодной поляризации металла. [25] |
На рис. 1 показана кривая катодной поляризации, выражающая кинетику протекания коррозионного процесса. По оси ординат отложена плотность катодного тока / к, а по оси абсцисс - изменение потенциала в отрицательную сторону от его равновесного значения. [26]
На рис. 120 приведены кривые катодной поляризации золота и сплава Аи - Ag - Си из щелочного цианистого электролита. [28]
На рис. 25 приведены кривые катодной поляризации железа, полученные в буферном растворе ( рН 9) в присутствии нитрита натрия. Восстановление аниона азотистой кислоты должно было бы привести к значительному увеличению предельного диффузионного тока, так как, кроме кислорода, в восстановительном процессе участвовали бы анионы. Однако экспериментальные данные показывают, что предельный диффузионный ток как в присутствии нитрита натрия, так и в его отсутствии, остается одним и тем же. [29]
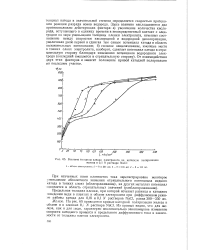 |
Влияние то / щины пленки электролита на катодную поляризацию железа в 0 1 Л растворе NaCl. [30] |
Страницы: 1 2 3 4 5