Кривая - адсорбция
Cтраница 1
Кривая адсорбции, построенная по уравнению ( XIII. При этом а практически не изменяется с изменением концентрации С. [1]
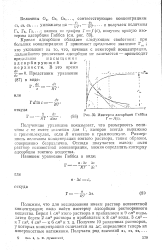 |
Изотерма адсорбции Гиббса Г / ( с. [2] |
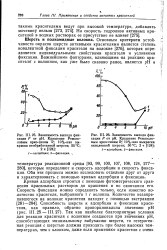
Кривая адсорбции обладает следующим свойством: при больших концентрациях Г принимает предельное значение Г; это указывает на то, что, начиная с некоторой концентрации, дальнейшего увеличения адсорбции не замечается - происходит предельное насыщение адсорбирующей поверхности. [3]
Кривая адсорбции для системы - NaCl - UC13 имеет максимум для расплавов, содержащих 10 - 12 мол. Кривая адсорбции для расплавов КС1 - UC13 имеет два максимума, значительно отличающихся по величине. Первый максимум соответствует 18 - 22 мол. Кривая адсорбции для расплавов КС1 - UC14 имеет вид с двумя максимумами, значительно отличающимися по величине. [4]
Кривая адсорбции строится с помощью фотометрического сравнения красильных растворов до крашения и по окончании его. Скорость фиксации можно определить только, если известно количество красителя, выбранного 1 г волокна. [6]
Кривая адсорбции I, представленная на рисунке 80, может быть обоснована теоретически. Лэнгмюр вывел уравнение, описывающее кривую этого типа. Пусть адсорбция происходит на однородной поверхности и ограничивается мономолекулярным слоем. Каждому давлению в газовой фазе отвечает определенная доля занятой поверхности, что является результатом установления динамического равновесия, при котором скорость адсорбции молекул в результате соударений с поверхностью равна скорости, с которой адсорбированные молекулы испаряются ( десорбируются) с поверхности в газовую фазу. [7]
Исследуя кривую адсорбции ( см. рис. 59), мк пришли к выводу, что Г сфемится к некоторой предельной величине Гто. [8]
Изучая кривую адсорбции, нетрудно заметить, что наиболее полное удаление растворенного вещества происходит при малых концентрациях раствора ( быстрый рост кривой от нуля); этим и следует пользоваться на практике. При больших же концентрациях выгодность применения адсорбции сильно ослабляется. [9]
 |
Определение констант. [10] |
Теперь рассчитывается кривая адсорбции для произвольных с ( табл. 16), что можно сделать непосредственно по прямой рис. 16, но не далее точки А, за пределами которой линейная зависимость нарушается. [11]
Аналогичным образом спрямляется кривая адсорбции, описываемая уравнением Лангмюра ( стр. [12]
Мы видим, что кривая адсорбции НС1 и кривая адсорбции H2S04 проходят совершенно параллельно. [13]
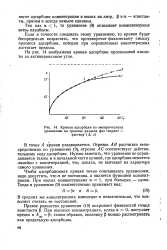 |
Кривая адсорбции по эмпирическому. [14] |
На рис. 14 изображена кривая адсорбции пропионовой кислоты на активированном угле. [15]
Страницы: 1 2 3 4