Поляризационная кривая
Cтраница 2
Поляризационные кривые анодного и катодного процессов находят из аналитических измерений, причем определяют, например, выделяющийся при различной поляризации водород или поступающее в раствор количество железа и выражают их в эквивалентных значениях тока. [16]
Поляризационные кривые указывают на анодную пассивность в растворах бикарбонатов натрия и кальция. [17]
Поляризационные кривые изображены на рис. 9.10: кривые ki и &2 относятся к золотым катодам, кривая k3 - к амальгамированным золотым электродам со стадиями Н202 ( 1а) и ОН ( 1а 1б); контрольные кривые k, k % и fe относятся к бескислородным растворам. [19]
Поляризационные кривые имеют асимптотический характер. Поэтому полной защиты железа при этом достичь нельзя; незначительное растворение, соответствующее значению / ар все же происходит. [20]
 |
Осциллограмма изменения потенциала твердого галлия во время излома в растворе, содержащем 58 г / л Ga и 196 г / л КОН, при 5 С и различных плотностях тока. [21] |
Поляризационные кривые, снятые на твердом галлиевом электроде, воспроизводятся значительно лучше, чем на жидком, что связано с более стабильным состоянием поверхности электрода. [22]
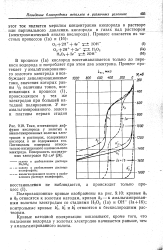
Поляризационные кривые для меди М4 и латуни Л62 представлены на рис. III. Анодная поляризация при растворении меди наблюдается лишь при малых плотностях тока; с увеличением значений плотности тока растворение меди и латуни происходит без какой-либо поляризации. Восстановление кислорода при потенциалах от 0 до 0 5 в протекает на меди легче, чем на латуни. Однако при более отрицательных потенциалах, когда становится возможным восстановление водорода, этот процесс протекает с большей скоростью на латуни. [23]
Поляризационные кривые измеряют обычно в прямоугольном электролизере, обеспечивающем равномерное распределение тока на электродах, с помощью определенным образом расположенного у поверхности электрода стеклянного капилляра. Близкое расположение зонда у электрода приводит к дополнительным методическим трудностям, подробное рассмотрение которых изложено в главе IV данной части. [24]
Поляризационные кривые, приведенные на рис. 111, наглядно показывают, что повышение температуры раствора заметно ускоряет электродную реакцию при потенциалах, соответствующих как горизонтальной, так и вертикальной ветвям кривой. На протяжении всего горизонтального участка кривой эффективность действия температуры остается примерно одинаковой, и при ее повышении на 40 процесс ускоряется приблизительно в 4 раза. [25]
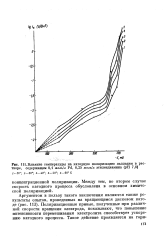 |
Влияние температуры на катодную поляризацию палладия в растворе, содержащем 0 1 моль / л Pd, ( моль / л этилендиамина ( рН 7 8. [26] |
Поляризационные кривые, полученные при различной скорости вращения электрода, показывают, что повышение интенсивности перемешивания электролита способствует ускорению катодного процесса. [27]
 |
Схема установки для снятия поляризационных кривых гальваностатическим методом.| Схема с нулевым сопротивлением для измерения силы тока пары. [28] |
Поляризационные кривые используются, как уже указывалось, и для количественного расчета скорости коррозии. Предложено много способов для такого расчета. Наиболее прост метод экстраполяции поляризационной кривой к стационарному потенциалу. При этом способе зависимость потенциала от плотности тока выражают в полулогарифмических координатах. [29]
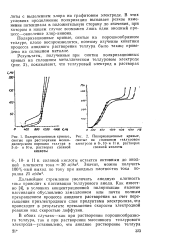 |
Поляризационные кривые, [ IMAGE ] Поляризационные кривые. [30] |
Страницы: 1 2 3 4 5