Реальная поляризационная кривая
Cтраница 1
Реальные поляризационные кривые ( см. рис. 9) начинают свой ход от стационарного значения электродного потенциала металла Уст в данной среде и фактически являются продолжением идеальных поляризационных кривых, которые берут начало от обратимых электродных потенциалов анодной и катодной реакции данного коррозионного элемента ( V A и V K) - Реальные поляризационные кривые ( катодные и анодные) наносят на коррозионную диаграмму и по их форме и взаимному расположению судят не только о максимально возможной величине коррозионного тока в данных условиях, но и о возможности торможения коррозионного процесса. Таким путем выявляется тот этап коррозионного процесса, который протекает с наибольшим затруднением и контролирует скорость разрушения металла в данной среде. Все защитные мероприятия направлены на то, чтобы усилить тормозящее действие контролирующего фактора. [1]
 |
Реальные поляризационные кривые для электродов макроэлемента медь - железо. Электролит 0 1 - н. NaCl, толщина слоя электролита 200 мкм. [2] |
Реальные поляризационные кривые наглядно показывают, что при контактной коррозии ввиду разной поляризуемости металлов, составляющих гальваническую пару, не может быть симметричности в распределении плотности тока на электродах. [3]
 |
Реальные поляризационные кривые для электродов макроэлемента медь - железо. Электролит 0 1 - н. NaCl, толщина слоя электролита 200 мкм. [4] |
На основании реальных поляризационных кривых, представленных на рис. 45, были рассчитаны константы поляризации электродов. [5]
В связи с этим необходимо было получить реальные поляризационные кривые для электродов данного элемента. [6]
Таким образом, метод состоит в измерении реальных поляризационных кривых V / ( /) в ешн ( пунктирная кривая на рис. 191) и определении тока саморастворения металла ( по коррозионным потерям Дт) / внутр при различных постоянных значениях потенциала V const с применением потенциостата. [7]
Имея эти данные, можно было построить реальную поляризационную кривую и по плотности тока найти поляризационные характеристики для различных участков анода и катода. [8]
В связи, с этим необходимо было получить реальные поляризационные кривые для электродов данного элемента. [9]
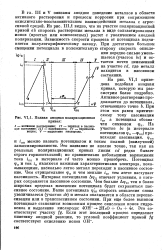 |
Полная анодная поляризационная кривая. [10] |
Это название не вполне точно, так как на реальных поляризационных кривых линия cd редко бывает строго горизонтальной; но сравнительно небольшими вариациями тока гпп в интервале cd часто можно пренебречь. Потенциал фп и ток гп являются важными характеристиками электрода, показывающими, насколько легко металл переходит в пассивное состояние. Чем отрицательнее рп и чем меньше in, тем легче наступает пассивность. Интервал потенциалов Дрп отвечает условиям, в которых сохраняется пассивное состояние. [11]
До последнего времени считалось, что при расчете поля учесть реальную поляризационную кривую очень сложно. Применение электронно-вычислительных машин ( ЭВМ) позволяет по-новому подойти к этой проблеме. [12]
Возможность практического использования полученного соотношения для определения деформационного изменения тока коррозии обосновывается так же, как и в известном методе снятия реальных поляризационных кривых для определения скорости коррозии металла на основе кинетической теории коррозии: идеальные поляризационные кривые, определяющие стационарный потенциал и ток коррозии, рассматриваются как продолжение тафелевских участков реальных поляризационных кривых. Это, очевидно, справедливо для электрохимически гомогенной поверхности, но также может быть принято для технических металлов ( железа, никеля, свинца и Др. На рис. 59 реальные поляризационные кривые показаны сплошными линиями. Для практического расчета скорости коррозии в формулу ( 232) следует подставлять величины сдвигов потенциалов, определенные сечением реальных анодных и катодных поляризационных кривых для произвольно выбранного значения плотности тока гальваностатической поляризации в пределах тафелевских участков. Из соотношения ( 229) видно, что изменение стационарного Потенциала вследствие деформации электрода не является однозначной функцией термодинамического состояния металла ( обу-словливающего анодное поведение) из-за участия катодного про-щесса. [13]
Возможность практического использования полученного соотношения для определения деформационного изменения тока коррозии обосновывается так же, как и в известном методе снятия реальных поляризационных кривых для определения скорости коррозии металла на основе кинетической теории коррозии: идеальные поляризационные кривые, определяющие стационарный потенциал и ток коррозии, рассматриваются как продолжение тафелевских участков реальных поляризационных кривых. На рис. 66 реальные поляризационные кривые показаны сплошными линиями. Для практического расчета скорости коррозии в формулу ( 245) следует подставлять величины сдвигов потенциалов, определенные сечением реальных анодных и катодных поляризационных кривых для произвольно выбранного значения плотности тока гальваностатической поляризации в пределах тафелевских участков. [14]
 |
Реальные ( 1 и 2 и идеальные ( 3 и 4 поляризационные кривые. [15] |
Страницы: 1 2 3