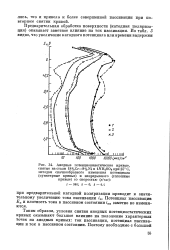
Анодная потенциостатическая кривая
Cтраница 1
Анодная потенциостатическая кривая для углеродистой стали в серной кислоте такой концентрации не имеет явно выраженного максимума. Для начальной пассивации нужна плотность тока всего в 5 - 10 раз выше, чем в полностью пассивном состоянии. Поэтому допустима установка в хранилище одного катода, расположенного в середине. Использовавшийся при защите катод ( рис. XIV. [1]
На анодной потенциостатической кривой для углеродистой стали в серной кислоте такой концентрации отсутствует явно выраженный максимум, соответствующий критической плотности тока пассивации. [2]
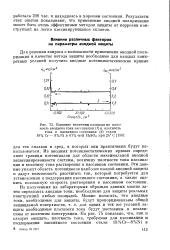 |
Влияние величины площади на плотность анодного тока пассивации ( 1 и плотность тока в пассивном состоянии ( 2 стали 18 % Сг - 8 % № в 67 % - ной H2S04 при 24 С. [3] |
Из анодных потенциостатических кривых определяют границы потенциалов для области максимальной анодной запассивированности системы, величину плотности тока пассивации и величину тока растворения в пассивном состоянии. Эти данные укажут область потенциалов наиболее полной анодной защиты и дадут возможность рассчитать ток, который потребуется для установления и поддержания пассивного состояния, а также оценить возможную скорость растворения в пассивном состоянии. Из полученных на лабораторных образцах данных можно затем определить анодные токи, необходимые для защиты реальных конструкций любых площадей. [4]
Из анализа анодной потенциостатической кривой становится ясно, какими путями можно ускорить коррозионный процесс. [5]
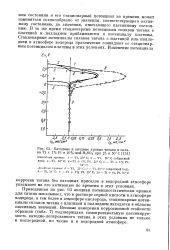 |
Катодные и анодные кривые титана и сплава Ti с 1 % Pt в 40 % - hohH2SO4 при 25 и 50 С Катодные кривые. 1 - Ti, 25 С. 2 - Ti, 25 С ( обратный ход. г - Ti, 50 С. 4 - Ti 1 % Pt, 25 С. 5 - Ti 1 % Pt. [6] |
Приведенная на рис. 63 анодная потенциостатическая кривая для титана показывает, что в растворе серной кислоты в атмосфере водорода, а тем более в атмосфере кислорода, стационарные потенциалы сплавов титана с платиной и палладием находятся в области пассивных значений. Весовые измерения коррозионной стойкости образцов ( табл. 7) подтверждают самопроизвольную пассивируе-мость катодно-легированного титана в этих условиях не только в кислородной, но также и в водородной атмосфере. [7]
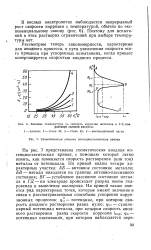 |
Влияние температуры на скорость коррозии металлов в 5 % - ном растворе соляной кислоты. [8] |
На рис. 7 представлена схематическая анодная потенциостатическая кривая, с помощью которой легко понять, как изменяется скорость растворения ( или ток) металла от потенциала. На кривой видны четыре характерных участка: АБ - активное состояние металла; БВ - металл находится на границе активно-пассивного состояния; ВГ - устойчивое пассивное состояние металла и ГД - на электроде происходят разряд ионов гид-роксила и выделение кислорода. [9]
Таким образом, условия снятия анодных потенциостатических кривых оказывают большое влияние на положение характерных точек на анодных кривых: ток пассивации, потенциал пассивации и ток в пассивном состоянии. [11]
В и охватывает все характерные области анодной потенциостатической кривой: активную, пассивную и транспассивную. Такая закономерность является общей для всех видов локальной коррозии и наблюдается, например, при изучении коррозионного растрескивания коррозионно-стойких сталей в хлоросоде ржащих средах. [12]
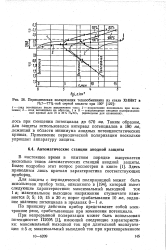 |
Периодическая поляризация теплообменника из стали Х18Н9Т в. [13] |
Таким образом, для защиты использовался интервал потенциалов в 180 мв, лежащий в области минимума анодных потенциостатических кривых. Применение периодической поляризации несколько упрощает аппаратуру защиты. [14]
Описанные опыты с титановым электродом повторили также в ат - мосфере аргона, и было установлено, что нет заметного отличия в ходе анодных потенциостатических кривых в условиях обновления поверхности по сравнению с кривыми, полученными в воздушной атмосфере. [15]
Страницы: 1 2 3